инструкция по применению таблеток и для чего он нужен, цена, отзывы, аналоги
- Беременность
- Развитие плода по неделям
- 1 триместр
- Скрининг 1 триместр
- 1-6 недели
- 1 неделя
- 2 неделя
- 3 неделя
- 4 неделя
- 5 неделя
- 6 неделя
- 7-12 недели
- 7 неделя
- 8 неделя
- 9 неделя
- 10 неделя
- 11 неделя
- 12 неделя
- 2 триместр
- Скрининг 2 триместра
- 13-18 недели
- 13 неделя
- 14 неделя
- 15 неделя
- 16 неделя
- 17 неделя
- 18 неделя
- 19-24 недели
- 19 неделя
- 20 неделя
- 21 неделя
- 22 неделя
- 23 неделя
- 24 неделя
- 3 триместр
- Скрининг 3 триместра
- 25-30 недели
- 25 неделя
- 26 неделя
- 27 неделя
- 28 неделя
- 29 неделя
- 30 неделя
- 31-36 недели
- 31 неделя
- 32 неделя
- 33 неделя
- 34 неделя
- 35 неделя
- 36 неделя
- 37-39 недели
- 37 неделя
- 38 неделя
- 39 неделя
- 37, 38, 39 недели у повторнородящих
- 1 триместр
- Как определить беременность
- Месячные и беременность
- Вопросы и рекомендации по беременности
- Выделения при беременности
- Питание при беременности
- Осложнения и боли при беременности
- Прерывание беременности
- Развитие плода по неделям
- Болезни
- Грипп Мичиган
- Рахит у грудничков
- Кишечная колика
- Пупочная грыжа
- Инструкции
- для детей
- при ОРВИ
- Виферон свечи
- Ибуклин Юниор
- Синупрет капли
- при кашле
- Аскорил сироп
- Бромгексин таблетки
- Пантогам сироп
- Синекод
- Саб симплекс
- Эриспирус сироп
- Эреспал сироп
- при гриппе
- Амоксиклав
- Амиксин
- Арбидол
- Панавир
- Ремантадин
- Тамифлю
- Циклоферон
- жаропонижающие
- Нурофен детский
- Панадол сироп
- Парацетамол сироп
- Цефекон свечи
- при болях
- Плантекс (от коликов)
- Смекта (от диареи)
- Энтерол (для кишечника) для детей
- Эспумизан беби (боли животика)
- Другие заболевания
- Вибуркол свечи (симптоматическое средство)
- Зиннат суспензия (отиты и т.
 п.)
п.) - Изофра (риниты и синуситы)
- Мирамистин (антисептик)
- Отипакс (отит)
- Сиалор (ЛОР-заболевания)
- при ОРВИ
- при беременности и лактации
- при ОРВИ
- Анальгин
- Пиносол
- Тизин
- при кашле
- Биопарокс
- Гексорал спрей
- Лизобакт
- Либексин
- Сироп Алтея
- Стодаль
- Фарингосепт
- Цикловита
- при гриппе
- Арбидол
- Ацикловир
- Ремантадин
- Тамифлю
- жаропонижающие
- Ибупрофен
- при болях
- Ибупрофен
- Но-шпа
- Пенталгин
- Цитрамон
- Другие заболевания
- Клотримазол (грибок, инфекция половых органов)
- Линдинет 20 (противозачаточное)
- Мастодинон (нарушение менструации)
- Норколут (гормональный препарат)
- Полижинакс (противогрибковое)
- Тироксин (при гипотиреозе)
- Эстровэл (от женских заболеваний)
- Ярина (противозачаточное)
- при ОРВИ
- для взрослых
- при ОРВИ
- Амиксин
- Арбидол
- Гриппферон
- Интерферон
- Кипферон свечи
- Ротокан
- Ремантадин
- Синупрет
- Тамифлю
- при кашле
- АЦЦ
- Либексин
- Ренгалин
- Стоптуссин
- Стодаль
- при гриппе
- Амиксин
- Дибазол
- Кагоцел
- Лавомакс
- Ремантадин
- Флемоксин Солютаб
- Цефтриаксон
- жаропонижающие
- Индометацин
- Ибупрофен
- Ринза
- при болях
- Колофорт (для пищеварительного тракта)
- Кеторол
- Мовалис (противовоспалительное)
- Найз таблетки
- Тримедат (для кишечника)
- Невролгии, ЦНС, головной мозг
- Аспаркам
- Актовегин
- Комбилипен
- Нейромультивит
- Циннаризин
- Другие заболевания
- Адвантан (дерматологические заболевания)
- Азитромицин (ЛОР-заболевания)
- Диазолин (от аллергии)
- Лоратадин (при аллергии)
- Овесол (для печени)
- Эссенциале форте Н (для печени)
- Полидекса (ЛОР-заболевания)
- Клотримазол (грибок, инфекция половых органов)
- Циклоферон (инфекционные, бактериальные, грибковые заболевания)
- при ОРВИ
- для детей
- Грудное вскармливание
- Питание при ГВ
- Кормление грудью
- Таблетки при ГВ
- Болезни при ГВ
- Прикорм грудничка
- Вопросы и рекомендации
- Калькуляторы
- Калькулятор ХГЧ
- Спермограмма: расшифровка результата
- Календарь овуляции для зачатия
- Срок беременности по неделям и дням
- Дата родов по месячным, дате зачатия
- Календарь беременности по неделям
- Рассчитать пол ребенка
- Калькулятор роста и веса ребенка
Поиск
- Инструкции по применению (по алфавиту):
АКТОВЕГИН гель — инструкция по применению, дозировки, аналоги, противопоказания
Клинико-фармакологическая группа
Препарат, улучшающий трофику и регенерацию тканей, для наружного применения
Форма выпуска, состав и упаковка
◊ Гель для наружного применения 20% однородный, бесцветный или желтоватого цвета, прозрачный.
| 100 г | |
| компоненты крови — депротеинизированный гемодериват из крови телят | 20 мл, |
| что соответствует содержанию сухой массы | 800 мг |
Вспомогательные вещества: кармеллоза натрия — 1.80 г, пропиленгликоль — 2.00 г, кальция лактат — 0.30 г, метилпарагидроксибензоат — 0.175 г, пропилпарагидроксибензоат — 0.025 г, вода очищенная — 94.90 г.
20 г — тубы алюминиевые (1) — коробки картонные.
30 г — тубы алюминиевые (1) — коробки картонные.
50 г — тубы алюминиевые (1) — коробки картонные.
100 г — тубы алюминиевые (1) — коробки картонные.
Фармакологическое действие
Актовегин — антигипоксант, активирует метаболизм глюкозы и кислорода.
Актовегин вызывает увеличение клеточного энергетического метаболизма. Его активность подтверждается увеличением потребления и повышением утилизации глюкозы и кислорода клетками. Эти два эффекта сопряжены, они вызывают увеличение метаболизма АТФ и, следовательно, повышают энергетический обмен.
Показания
— раны и воспалительные заболевания кожи и слизистых оболочек: ожоги (в т.ч. солнечные), порезы кожи, ссадины, царапины, трещины;
— с целью улучшения регенерации ткани после ожогов, в т.ч. после ожога кипящей жидкостью или паром;
— в качестве начальной терапии мокнущих язв;
— для профилактики и лечения реакций со стороны кожи и слизистых, обусловленных воздействием радиации;
— для предварительной обработки раневых поверхностей перед трансплантацией кожи при лечении ожоговой болезни.
Противопоказания
— гиперчувствительность к препарату Актовегин или аналогичным препаратам.
Дозировка
Наружно.
Гель наносится тонким слоем на пораженные участки несколько раз в день. Для очищения язвенных поверхностей наносится толстый слой геля и закрывается компрессом с 5% мазью Актовегин или марлевой повязкой, пропитанной мазью. Повязку меняют один раз в сутки, при лечении сильно мокнущих поверхностей — несколько раз в сутки. В дальнейшем лечение следует продолжить Актовегин 5% в форме крема или Актовегином 5% в форме мази.
Повязку меняют один раз в сутки, при лечении сильно мокнущих поверхностей — несколько раз в сутки. В дальнейшем лечение следует продолжить Актовегин 5% в форме крема или Актовегином 5% в форме мази.
Побочные действия
Обычно препарат переносится хорошо.
В начале лечения препаратом Актовегин 20% гель могут возникнуть местные болевые ощущения, связанные с местным отеком тканей. Однако это не является свидетельством непереносимости препарата. В случае, если болевые ощущения сохраняются или ожидаемый эффект от препарата не достигнут, следует обратиться к врачу.
У пациентов, имеющих в анамнезе реакции гиперчувствительности, в редких случаях могут развиваться аллергические реакции.
Лекарственное взаимодействие
Взаимодействие с другими лекарственными препаратами в настоящее время неизвестно.
Беременность и лактация
Применение при беременности и лактации допускается.
Условия отпуска из аптек
Препарат разрешен к применению в качестве средства безрецептурного отпуска.
Условия и сроки хранения
Препарат хранить в месте, недоступном для детей при температуре не выше 25°С.
Срок годности — 3 года. Не использовать по истечении срока годности.
Описание препарата АКТОВЕГИН основано на официально утвержденной инструкции по применению и утверждено компанией–производителем.
Предоставленная информация о ценах на препараты не является предложением о продаже или покупке товара. Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в соответствии со статьей 55 ФЗ «Об обращении лекарственных средств».
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
Актовегин раствор для инъекций 400мг: инструкция, отзывы, аналоги, цена в аптеках
Cостав
действующее вещество: 1 мл препарата содержит депротеинизований гемодериват из крови телят, соответствует 40 мг сухой массы
вспомогательные вещества: натрия хлорид, вода для инъекций.
Лекарственная форма
Раствор для инъекций.
Основные физико-химические свойства: раствор желтоватого цвета.
Фармакологическая группа
Средства, влияющие на пищеварительную систему и метаболические процессы. Код АТХ А16А Х.
Фармакологические свойства
Фармакодинамика.
Препарат Актовегин является депротеинизований гемодериват из крови телят, содержащий только физиологические вещества с молекулярной массой менее 5000 дальтон. Действие препарата проявляется нейропротективного и метаболическими эффектами. Нейропротективные эффекты обеспечиваются уменьшением повреждающего воздействия оксидативного стресса и уменьшением апоптоза нейронов. Метаболические эффекты являются органонеспецифичные. На молекулярном уровне Актовегин способствует ускорению процессов утилизации кислорода (повышает устойчивость к гипоксии) и глюкозы, тем самым способствует повышению энергетического метаболизма. Суммарный эффект этих процессов заключается в усилении энергетического состояния клетки, особенно в условиях гипоксии и ишемии.
У пациентов с сахарным диабетом 2-го типа и диабетической полинейропатией Актовегин уменьшает интенсивность симптомов диабетической полинейропатии (колющая боль, жжение, парестезии, онемение в нижних конечностях). Уменьшает нарушения вибрационной чувствительности и улучшает качество жизни пациентов.
Фармакокинетика.
С помощью фармакокинетических методов невозможно изучить фармакокинетические характеристики препарата Актовегин (абсорбция, распределение и элиминация активных ингредиентов), поскольку он состоит только из физиологических компонентов, которые обычно имеются в организме.
Показания
- Заболевания головного мозга сосудистого и метаболического генеза (в том числе деменция).
- Нарушение периферического (артериального, венозного) кровообращения и их осложнения (артериальная ангиопатия, венозная трофическая язва).

- Диабетическая полинейропатия (ДПН).
Противопоказания
Гиперчувствительность к любым компонентам препарата или к препаратам подобного состава. Декомпенсированная сердечная недостаточность, отек легких, олигурия, анурия являются общими противопоказаниями к инфузионной терапии, поэтому введение препарата в виде инъекций при этих состояниях противопоказано ввиду возможного гипергидратацию.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Данных о взаимодействии Актовегина с другими препаратами нет.
Особенности применения
Внутримышечно желательно вводить не более 5 мл, так как раствор является гипертоническим.
Раствор для инъекций совместим с 0,9% раствором натрия хлорида и 5% раствором глюкозы.
Препарат Актовегин, раствор для инъекций, следует применять в стерильных условиях. Поскольку препарат не содержит консервантов, содержимое ампулы предназначен для однократного использования. Открытые ампулы и готовый раствор следует немедленно использовать. Неиспользованный продукт и отходы следует утилизировать в соответствии с местными требованиями.
Неиспользованный продукт и отходы следует утилизировать в соответствии с местными требованиями.
В связи с возможностью возникновения анафилактических реакций рекомендуется провести пробную инъекцию (тест на чувствительность). В случае развития нарушений водно-электролитного обмена (например, гиперхлоремии, гипернатриемии) необходимо провести соответствующую коррекцию.
Раствор для инъекций имеет слегка желтоватый оттенок. Интенсивность окраски может варьировать от одной партии к другой в зависимости от особенностей использованных исходных материалов, однако это не сказывается негативно на активности препарата или чувствительности к нему.
Можно использовать только прозрачный раствор без видимых частиц.
Раствор содержит натрий. Это следует учитывать пациентам, которые находятся на контролируемой натриевой диете.
Применение в период беременности или кормления грудью.
Препарат применять в период беременности и кормления грудью только тогда, когда ожидаемая польза для матери превышает возможный риск для плода или ребенка. Во время применения препарата Актовегин при плацентарной недостаточности, хотя и редко, наблюдались летальные случаи, которые могли быть следствием основного заболевания. Применение препарата Актовегин в период кормления грудью не сопровождалось негативными эффектами ни для матери, ни для ребенка.
Во время применения препарата Актовегин при плацентарной недостаточности, хотя и редко, наблюдались летальные случаи, которые могли быть следствием основного заболевания. Применение препарата Актовегин в период кормления грудью не сопровождалось негативными эффектами ни для матери, ни для ребенка.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Актовегин не имеет или имеет очень незначительное влияние на способность управлять автотранспортом или другими механизмами. Однако, следует учитывать возможные проявления побочного действия со стороны нервной системы (см. Раздел «Побочные реакции»).
Способ применения и дозы
Актовегин, раствор для инъекций, применять внутривенно (струйно, капельно), внутриартериально по 5-20 мл в сутки.
Внутримышечно вводить медленно, не более 5 мл в сутки.
Для внутривенного введения препарат разводить в 0,9% растворе натрия хлорида или 5% растворе глюкозы. Допускается конечная концентрация Актовегина — до 2000 мг сухого вещества на 250 мл раствора.
дозировка:
а) обычная рекомендованная доза
учитывая клиническую симптоматику, сначала вводить 5-10 мл внутривенно или внутриартериально, далее — по 5 мл внутривенно или медленно внутримышечно ежедневно или несколько раз в неделю
б) дозы в зависимости от показаний для применения:
При тяжелых состояниях
Внутривенно капельно вводить 20-50 мл / сут Актовегина в течение нескольких дней до достижения выраженного клинического эффекта.
Состояние средней тяжести или обострения хронических заболеваний
5-20 мл / сут внутривенно или внутримышечно в течение 14-17 дней.
Курс планового лечения
2-5 мл / сут внутривенно или внутримышечно в течение 4-6 недель.
Количество введений — от 1 до 3 раз в зависимости от степени тяжести.
При диабетической полинейропатии
Лечение начинать с внутривенного применения препарата в дозе 2 г в сутки в течение 3 недель с последующим переходом на таблетки — 2-3 таблетки 3 раза в сутки не менее 4-5 месяцев.
Дети. Данные по применению препарата у детей отсутствуют, поэтому препарат не рекомендуется применять этой категории пациентов.
Передозировка
Случаи передозировки препаратом Актовегин неизвестны.
Побочные реакции
Ниже описаны побочные реакции, которые могут возникать у пациентов в результате применения препарата Актовегин. Возможно возникновение анафилактических (аллергических) реакций, которые могут проявляться:
со стороны иммунной системы и кожи — возможные реакции гиперчувствительности, включая аллергические реакции, анафилактические и анафилактоидные реакции вплоть до развития анафилактического шока, повышение температуры тела, озноб, ангионевротический отек, гиперемия кожи, кожные высыпания, зуд, крапивница, повышенная потливость, отеки кожи и / или слизистых оболочек, приливы жара, изменения в месте введения
со стороны пищеварительного тракта — диспепсические явления, включая боль в эпигастральной области, тошнота, рвота, диарея;
со стороны сердечно-сосудистой системы — боль в области сердца, увеличение частоты сердечных сокращений (тахикардия), одышка, акроцианоз, бледность кожи, артериальная гипотензия или гипертензия,
со стороны дыхательной системы — увеличение частоты дыхания, чувство сжатия в грудной клетке, затрудненное глотание и / или дыхания, боль в горле, приступ удушья;
со стороны нервной системы — головная боль, общая слабость, головокружение, потеря сознания, возбуждение, дрожь (тремор), парестезии
со стороны костно-мышечной системы — боль в мышцах и / или суставах, боль в пояснице.
В таких случаях лечение препаратом Актовегин необходимо прекратить и применить симптоматическую терапию.
Срок годности
5 лет.
Условия хранения
Хранить при температуре не выше 25 ° С в оригинальной упаковке. Хранить в недоступном для детей месте!
Несовместимость
Препарат не следует смешивать в одной емкости с другими растворами, за исключением указанных в разделе «Способ применения и дозы».
Упаковка
По 2 мл в ампуле; по 25 ампул в картонной коробке.
По 5 мл в ампуле; по 5 ампул в картонной коробке
По 10 мл в ампуле; по 5 ампул в картонной коробке.
Категория отпуска
По рецепту.
Производитель
ООО «Кусум Фарм», Украина / LLC «Kusum Pharm», Ukraine.
(Упаковка
Актовегин уколы: состав, показания, свособы введения
Препарат Актовегин – лекарственное средство антигипоксического действия, активизирующее доставку кислорода и глюкозы в различные органы и ткани и способствующее их усвоению. Антигипоксический эффект Актовегина – универсальный ускоритель обмена веществ во всех системах органов. Местное или наружное использование препарата эффективно при заживлении ожогов, ссадин, порезов, язв, пролежней, других повреждений тканей. Средство позволяет уменьшить проявление нарушений, которые возникли в результате недостаточного кровоснабжения тканей и органов, переводит тяжёлые формы заболевания сосудов в более лёгкие, способствует улучшению памяти и мышления. Для ликвидации последствий инсульта, черепно-мозговых травм, для улучшения кровообращения сосудов головного мозга врачи советуют систематически применять Актовегин уколы, таблетки.
Антигипоксический эффект Актовегина – универсальный ускоритель обмена веществ во всех системах органов. Местное или наружное использование препарата эффективно при заживлении ожогов, ссадин, порезов, язв, пролежней, других повреждений тканей. Средство позволяет уменьшить проявление нарушений, которые возникли в результате недостаточного кровоснабжения тканей и органов, переводит тяжёлые формы заболевания сосудов в более лёгкие, способствует улучшению памяти и мышления. Для ликвидации последствий инсульта, черепно-мозговых травм, для улучшения кровообращения сосудов головного мозга врачи советуют систематически применять Актовегин уколы, таблетки.
Состав, форма выпуска и упаковка
Основной компонент – гемодериват депротеинизированный дозировкой 40мг Актовегина на 1 мл раствора для инъекций. Его получают из крови здоровых телят, которые питаются исключительно молоком. Препарат производится в таблетках, мазях и гелях, ампулах для постановки инъекций и растворах для капельниц. Кроме основного компонента, раствор содержит хлорид натрия и воду для инъекций.
Кроме основного компонента, раствор содержит хлорид натрия и воду для инъекций.
Раствор для инфузий выпускается в ампулах разной дозировки:
| Дозировка | Количество ампул (штук) | Объём |
| 400 мг | 5 | 10 мл |
| 200 мг | 5 | 5 мл |
| 80 мг | 25 | 2 мл |
Наружная упаковка для ампул изготовлена из картона, внутренняя – пластиковый контейнер. На картонной таре указаны серия производства и срок годности. В упаковку вложена инструкция (руководство) по применению. Прозрачный раствор имеет желтоватый цвет с разными оттенками в зависимости от серии выпуска. Цвет препарата никаким образом не отражается на эффективности препарата.
В аптеке можно купить также Актовегин в бутылках для капельницы объёмом 250 мл:
- на основе декстрозы с 10-процентным содержанием действующего вещества;
- на физрастворе с 10- и 20-процентным содержанием гемодеривата.

Фармакологические свойства и фармакокинетика
Фармакокинетические методы не позволяют изучить фармакологические свойства Актовегина, такие как абсорбция (всасывание), распределение и элиминация (разрушение и выведение) активных ингредиентов, потому что в составе препарата находятся физиологические компоненты, содержащиеся в самом организме.
Актовегин усиливает энергетический обмен, способствует быстрой переработке кислорода, защищает организм от кислородного голодания.
Результаты клинических исследований и опытов, проводимых на животных, показали, что препарат начинает действовать уже через полчаса после того, как поставили укол. Наибольший эффект после парентерального способа введения достигается через 3 часа, после перорального – от 2 до 6 часов.
Показания и противопоказания к применению
Препарат Актовегин применяется для лечения различных заболеваний как самостоятельно, так и вместе с другими лекарствами. Он широко используется в неврологии, кардиологии, хирургии, травматологии, дерматологии, гинекологии. Больными данное лекарство переносится легко, и организм быстрее восстанавливается.
Больными данное лекарство переносится легко, и организм быстрее восстанавливается.
Самолечение недопустимо! Только врач знает, когда, в каких дозировках и сколько дней колоть препарат.
Актовегин чаще применяется в уколах, чем в таблетках. Его назначают при заболеваниях, связанных с нарушениями кровообращения, обмена веществ и при повреждении кожи. Особенно инъекции Актовегина помогают в комплексном лечении:
- геморрагического или ишемического инсультов;
- энцефалопатии;
- церебральной недостаточности;
- артериальной ангиопатии;
- диабетической полинейропатии;
- эндартериита;
- инфаркта миокарда;
- болезни Альцгеймера;
- ухудшения памяти и внимания вследствие сосудистых нарушений;
- черепно-мозговых травм;
- слабоумия.
Препарат назначают при онемении, отекании или покалывании нижних конечностей.
Актовегин нашёл широкое применение в хирургии и дерматологии для лечения:
- пролежней и долго заживающих ран;
- трофических язв;
- лучевых поражений кожи;
- обморожений;
- термических ран и химических ожогов;
- для профилактики осложнений после операций на органах зрения.

На сегодняшний день инъекции Актовегина востребованы в косметологии:
- после пластических операций;
- подтяжки лица;
- ринопластики;
- для предотвращения осложнений и ускорения восстановительных процессов после увеличения груди, липосакции и так далее.
В составе препарата Актовегин содержатся естественные для организма вещества, поэтому он хорошо переносится при парентеральном (внутривенном) применении. Его назначают взрослым любого возраста, пожилым людям, детям. Основным противопоказанием к применению данного лекарства является индивидуальная непереносимость, поэтому перед его назначением необходимо сделать тест на восприимчивость препарата.
Использование инфузионного введения противопоказано больным с отёком легких, сердечной или почечной недостаточностью, задержкой жидкости в организме. Кроме этого, капельницы с Актовегином на основе декстрозы недопустимы диабетикам.
Считается, что препарат не оказывает отрицательного влияния на будущего ребёнка, поэтому его часто прописывают беременным и кормящим женщинам (хотя, согласно инструкции, беременность и период лактации относятся к противопоказаниям). В отдельных случаях, например, при нарушении кровоснабжения плаценты, гипоксии, несоответствии резус-фактора крови матери и плода, недоразвитии плаценты, тяжёлых хронических заболеваниях женщины инъекции Актовегина облегчают состояние беременной и могут спасти жизнь плоду.
В отдельных случаях, например, при нарушении кровоснабжения плаценты, гипоксии, несоответствии резус-фактора крови матери и плода, недоразвитии плаценты, тяжёлых хронических заболеваниях женщины инъекции Актовегина облегчают состояние беременной и могут спасти жизнь плоду.
Инструкция по применению
Актовегин нужно вводить внутривенно струйно либо капельно. Сначала препарат следует растворить в 0,9-процентном физрастворе или 5-процентном растворе глюкозы. Окончательная дозировка Актовегина составляет 2000 мг сухого вещества на 250 мл раствора.
Суточная доза Актовегина при внутриартериальном введении должна составлять 5-20 мл.
Разрешённая дозировка при внутримышечном введении не должна быть более 5 мл в сутки и производить её необходимо медленно.
Болезненный ли укол Актовегина? Смотря в каком виде его принимать. Если внутривенно, то болевые ощущения отсутствуют.
При внутримышечном введении препарат входит достаточно болезненно.
Приготовление раствора
Как лучше применять Актовегин – внутривенно или внутримышечно – зависит от тяжести заболевания. Препарат также можно добавлять в растворы для инфузий. Для этого в основной изотонический физиологический раствор (200-300 мл) или 5-процентный раствор глюкозы необходимо добавить 10-50 мл Актовегина (раствора для инъекций).
Рекомендованные дозы и передозировка
Для выполнения внутримышечных инъекций применяют не более 5 мл Актовегина. Вводить препарат нужно медленно, поскольку он является гипертоническим, то есть повышает давление.
Во время острого периода ишемического инсульта (5-й…7-й дни) Актовегин капают по 2000 мг в сутки внутривенно капельно до 20 инфузий, постепенно переходя на таблетки (2 таблетки 3 раза в сутки, то есть до 1200 мг в день). Общий курс лечения составляет 6 месяцев.
Лечение деменции (слабоумия, снижения умственной деятельности) – капельно внутривенно 2000 мг в сутки в течение месяца.
Нарушения периферического кровообращения и его последствия – по 800-2000 мг ежесуточно в вену на протяжении 4 недель.
Диабетическая полиневропатия – суточная норма 20 инфузий. То есть 2000 мг вводится внутривенно капельно, затем осуществляется переход на таблетированную форму (3 таблетки 3 раза в сутки, то есть 1800 мг) в течение 4-5 месяцев.
Передозировка препаратом Актовегин неизвестна.
Актовегин – как вводить внутривенно
Актовегин – раствор для внутривенного введения, колоть который должен только специалист с медицинским образованием. Чаще всего назначают одну инъекцию в сутки. Если нарушено мозговое кровообращение, врач назначает лечение в виде 10 мл лекарства в сутки в течение 2 недель, затем доза снижается до 5 мл, и лечение продолжается ещё месяц. При ишемическом инсульте применяют капельницу с 250-500 мл раствора, для заживления язв и серьёзных поражений кожи хватит одной ёмкости Актовегина для инфузивного введения. По инструкции курс лечения продолжается от 10 до 30 дней в зависимости от тяжести заболевания.
Как колоть Актовегин внутримышечно
Любой человек, имеющий медицинскую подготовку, может поставить Актовегин внутримышечно. Для этого нужно взять ампулу вертикально и постучать по ней, чтобы раствор скатился вниз. Затем отломить кончик и набрать препарат в шприц. Лучше всего колоть Актовегин в мышцу, где нет жировой прослойки, например, в ягодицу, верхнюю часть плеча, бедро.
Поскольку внутримышечные инъекции малоэффективны, их применяют в основном для лечения патологий средней тяжести – для быстрого заживления ран или комплексного лечения хронических заболеваний сосудов. В сутки допускается вводить не более 5 мл раствора внутримышечно.
Возможные побочные действия и осложнения
Многочисленные исследования показали, что пациенты хорошо переносят препарат, и побочные эффекты при его правильном использовании проявляются крайне редко. В основном, это аллергические реакции, вызванные индивидуальной непереносимостью препарата (зуд, крапивница, покраснение кожных покровов, высыпания).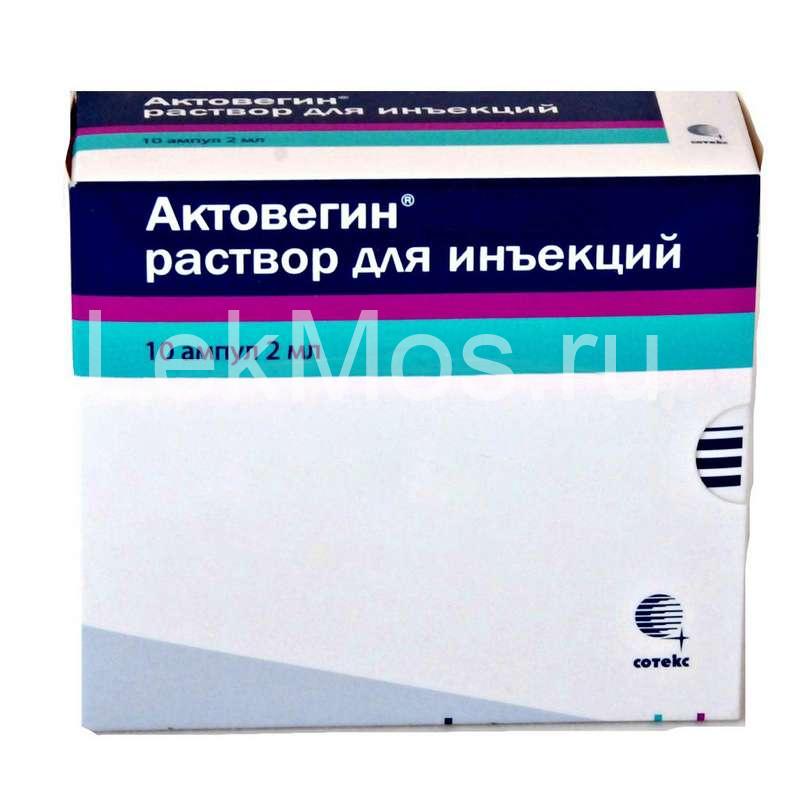 Тяжёлые случаи сопровождаются развитием ангионевротического отёка, возможен анафилактический шок, потому первый раз можно ввести не более 2 мл.
Тяжёлые случаи сопровождаются развитием ангионевротического отёка, возможен анафилактический шок, потому первый раз можно ввести не более 2 мл.
Побочные реакции со стороны пищеварительной, дыхательной и других систем:
- тошнота, рвота;
- диарея;
- тяжесть в желудке;
- одышка, затруднённое дыхание, тяжесть в груди;
- головная боль, слабость, головокружение;
- скачок артериального давления в сторону понижения или повышения;
- возможна потеря сознания;
- повышение температуры тела;
- проблемы с дыханием, удушье;
- сильное потоотделение;
- боль в области горла, трудно глотать;
- болезненные ощущения в сердце, пояснице, суставах;
- бледность кожи.
Боль, отёк, покраснение и образование уплотнений говорят о том, что препарат неправильно или слишком быстро ввели.
Особые указания по применению
В инструкции производитель Актовегина не указал особые рекомендации по приёму препарата.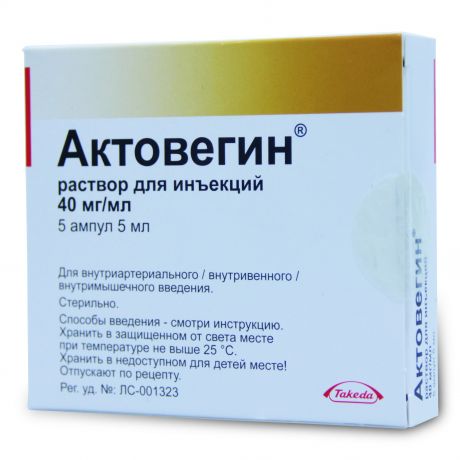 К примеру, при сахарном диабете пациент должен принимать лекарство под наблюдением врача, поскольку данное средство способно задерживать воду, что очень вредно для организма диабетика.
К примеру, при сахарном диабете пациент должен принимать лекарство под наблюдением врача, поскольку данное средство способно задерживать воду, что очень вредно для организма диабетика.
Кроме этого, раствор Актовегина относится к разряду гипертонических, поэтому его дозировка не должна превышать 5 мл в сутки.
Существует также риск получить анафилактический шок. Чтобы этого не произошло, каждому пациенту необходимо пройти предварительное тестирование на чувствительность организма к компонентам препарата. Проба выполняется внутримышечно путём инъецирования 2 мл раствора с последующим наблюдением за реакцией организма.
Лекарственные взаимодействия
В одной ёмкости (шприце, капельнице) раствор для инъекций Актовегин нельзя смешивать с другими растворами. Исключение составляют изотонические растворы глюкозы или хлорида натрия.
Можно ли колоть одновременно с Актовегином препарат Комбилипен? Да, можно. Противопоказания в этом случае отсутствуют, наоборот, их совместное применение способствует скорейшему выздоровлению. Комбипилен содержит комплекс витаминов группы В, он усиливает фармакологический эффект Актовегина.
Комбипилен содержит комплекс витаминов группы В, он усиливает фармакологический эффект Актовегина.
Информация о взаимодействии препарата с другими лекарственными средствами отсутствует.
Совместимость препарата и алкоголя
Большинство ноотропных медикаментозных препаратов, среди которых Актовегин, несовместимы с алкоголем, поскольку оказывают дополнительную нагрузку на почки и печень.
При нарушении функции почек и печени
Как было сказано раньше, препарат оказывает большую нагрузку на жизненно важные органы – печень и почки. Следовательно, для лечения невралгических либо других заболеваний необходимо использовать препараты-аналоги, у которых воздействие на органы выражено не так сильно.
Актовегин противопоказан при анурии, олигурии.
При беременности и лактации
Актовегин не стоит принимать беременных и кормящим женщинам, так как это может негативно отразиться на её гормональном фоне.
Препарат во время беременности и в период лактации назначают исключительно по жизненным показаниям.
Лечение детей
В инструкции к препарату не сказано, что Актовегин можно использовать для лечения детей. Однако неврологами данное средство часто назначается даже младенцам, которым едва исполнилось две недели. При этом препарат применяется именно в уколах, потому что так легче определиться с правильной дозировкой.
Актовегин назначают детям в том случае, если у них нарушено мозговое кровообращение, или наблюдается задержка умственного развития вследствие предродовой гипоксии, полученных при родоразрешении травм. Врач прописывает лечение данным препаратом, если замечает, что малыш подёргивает шеей, периодически у него возникают судороги и тики, если поставить его на ноги, то он опирается на пальчики. У старших детей это выражается в отставании умственного, физического, речевого развития, повышенной возбудимости.
Для каждого возраста ребёнка (до 6 лет) дозировка рассчитывается индивидуально:
- дети от года до трёх лет – на 1 кг веса 0,5 мл раствора в сутки;
- дети от 3 до 6 лет – 0,2-0,4 мл на 1 кг массы тела в сутки.

Уколы Актовегина ставят внутривенно или внутримышечно. Для того чтобы инъекция не была болезненной для ребёнка, рекомендуется развести препарат Новокаином в соотношении 2 мл Актовегина на 1,5 мл 0,5-процентного раствора.
Препарат имеет несколько аналогов подобного действия («Курантил», «Солкосерил», «Мексидол», «Церебролизин»), стоимость которых ниже цены оригинала. Однако Актовегин – самое эффективное средство, которым лечат серьёзные поражения кожи и нарушения мозгового кровообращения.
Условия отпуска из аптек
Актовегин продаётся только по рецепту.
Как хранить Актовегин в ампулах
Условия хранения раствора:
- в прохладном, закрытом от света месте;
- в оригинальной таре;
- при температуре не более 25 °С;
- в недоступном для детей месте;
- не более трёх месяцев.
Срок годности – 5 лет.
инструкция по применению внутримышечно, для чего назначают внутривенно в ампулах, показания взрослым, капельница помогает от, как лучше колоть инъекции, раствор побочные действия, можно ли струйно, дозировка 5 (2) мл, хранение, больной или нет, вводить 40 мг в вену, когда утром или вечером, препарат капельно пожилым людям, форма выпуска, болезненные эффекты, разводить лекарство, курс лечения
На чтение 7 мин. Просмотров 455
Просмотров 455
Для восстановления ткани и ускорения обмена веществ во всех органах больным назначают Актовегин (уколы). Состав, фармакологическое действие, дозировка и условия хранения ампул представлены в подробной инструкции.
Состав и действие лекарства
Актовегин в жидком состоянии подходит для уколов и капельниц. Активным компонентом является депротеинизированный гемодериват, который получают в результате очистки крови здоровых телят, кормящихся молоком, от крупных молекул белка. В процессе отделения остаются малые частицы, активизирующие метаболизм в человеческом организме и способствующие предотвращению развития аллергических реакций.
Жидкое средство в ампулах действует намного быстрее, чем таблетированное. Инъекции производятся в разных формах и количестве:
- раствор Актовегин для капельниц на глюкозе — в бутылях по 250 мл;
- для инфузии на 0,9% хлориде натрия на физрастворе — в бутылях по 250 мл;
- для инъекций — в ампулах по 2, 5 и 10 мл.

Количество действующего вещества в каждом лекарстве разное:
- В бутилированной форме:
- в растворах для инфузий на декстрозе — 4 мг/мл вещества, или 10%;
- в лекарствах для капельниц на 0,9% хлориде натрия на физрастворе — 4 мг/мл (10%) или 8 мг/мл (20%).
- В ампулах находится 40 мг сухого гемодеривата на 1 мл, соответственно:
- в 2 мл — 80 мг активного компонента;
- 5 мл — 200 мг;
- 10 мл — 400 мг.
В состав лекарственного средства дополнительно входят:
- в растворах для капельниц на глюкозе — вода, хлорид натрия и декстроза;
- для инфузий на физрастворе — хлорид натрия и вода;
- для инъекций Актовегина в ампулах — вода.
Медицинский препарат в ампулах — прозрачный, однородный, желтоватого оттенка, без осадка и примеси. При наличии мути и посторонних образований Актовегин колоть нельзя.
Актовегин — антигипоксант, который оказывает 3 вида фармакологических эффектов:
- Метаболический.
 Увеличивает поглощение и вывод кислорода и глюкозы из крови, улучшает энергетический метаболизм клеток, питание ткани, понижает формирование лактата при ишемии.
Увеличивает поглощение и вывод кислорода и глюкозы из крови, улучшает энергетический метаболизм клеток, питание ткани, понижает формирование лактата при ишемии. - Нейропротективный. Препятствует гибели клеток, улучшает состояние центральной и периферической нервной системы.
- Микроциркуляторный. Повышает скорость кровяного потока, уменьшает перикапиллярную зону, понижает миогенный тонус прекапиллярных артериол и капиллярных сфинктеров.
Общее терапевтическое действие препарата:
- Быстрое заживление любых повреждений кожи.
- Стимуляция кровообращения в кровеносной системе.
- Улучшение синтеза волокон коллагена.
- Уменьшение тканевой гипоксии и повышение усвояемости глюкозы.
- Увеличение энергообмена в сосудах головного мозга.
Для чего назначают уколы
Врачи назначают Актовегин взрослым людям при разных болезненных состояниях организма как в виде отдельных уколов, так и наряду с комплексной терапией. Лекарство помогает от неврологических, хирургических, кардиологических, гинекологических болезней, дерматологических повреждений кожи и при разных травмах.
Показания к применению:
- Болезни, связанные с нарушением кровотока в головном мозге:
- спутанность сознания, снижение умственных способностей, амнезия, понижение зрения, возникшие после черепно-мозговой травмы;
- инсульт ишемический;
- частые головные боли, шум и головокружение.
- Заболевания периферической, венозной, артериальной крови:
- атеросклероз артерий;
- дизорическая ангиопатия;
- ангионевроз;
- трофические язвы;
- вазопатии;
- облитерирующий эндартериит.
- Расстройства нервной системы.
- Кожные заболевания и поражения слизистых оболочек, полученные при термических, химических ожогах, ссадинах, порезах, после лучевой терапии при сильном радиационном облучении.
Актовегин лечит пролежни, обморожения, отекание, онемение нижних конечностей у пожилых пациентов. После косметических и пластических операций, связанных с подтяжкой лица, коррекцией формы носа, грудей и других частей тела, врачи рекомендуют сначала делать уколы, а затем принимать таблетки на основе гемодеривата для предотвращения осложнений и быстрого восстановления.
Согласно инструкции по применению, жидкий препарат детям вводить не рекомендуется из-за отсутствия полных данных о его использовании.
При замедленном физическом и умственном развитии после родовых травм, задержке речи, гиперактивности, постоянных судорогах и тиках неврологи назначают лечение уколами Актовегина внутривенно или в мышцу. По сравнению с таблетками инъекции позволяют правильно рассчитать нужную дозировку для ребенка.
Противопоказания
К противопоказаниям относят гиперчувствительность к лекарству. При отеке легких, анурии, олигурии Актовегин вводить внутривенно или внутримышечно нельзя. При сахарном диабете капельницы с Актовегином, в составе которого имеется декстроза, не делают.
Беременным и женщинам, кормящим грудью, инфузии запрещены. Бывают случаи, когда врач назначает лекарство для улучшения состояния перед родами и даже спасения ребенка, например, при нарушении движения крови в плаценте, резус-конфликте между плодом и матерью, гипоксии или плацентном недоразвитии.
Способ применения и дозы
Все процедуры выполняются в специализированном учреждении медицинским работником при полном контроле врача. Нельзя капать через капельницу, делать уколы внутримышечно или вводить Актовегин в вену самостоятельно. Перед основным курсом лечения вливают пробную дозу 2 мл. При отсутствии противопоказаний и аллергии, которые возможны при парентеральном применении, терапию в установленной врачом дозировке продолжают.
Лекарство вводят внутриартериально, внутримышечно или внутривенно, соблюдая инструкцию по применению Актовегина.
Какие по Вашему мнению наиболее важные факторы при выборе медицинского учреждения?Poll Options are limited because JavaScript is disabled in your browser.Доверие к врачу 73%, 1261 голос
1261 голос 73%
1261 голос — 73% из всех голосов
Современное оборудование 14%, 239 голосов
239 голосов 14%
239 голосов — 14% из всех голосов
Близкое расположение к дому 5%, 81 голос
81 голос 5%
81 голос — 5% из всех голосов
Советы знакомых 4%, 72 голоса
72 голоса 4%
72 голоса — 4% из всех голосов
Стоимость услуг 4%, 69 голосов
69 голосов 4%
69 голосов — 4% из всех голосов
Реклама 1%, 14 голосов
14 голосов 1%
14 голосов — 1% из всех голосов
Всего голосов: 1736
04. 11.2019
11.2019
×
Вы или с вашего IP уже голосовали.Можно ли колоть внутримышечно
Способ использования Актовегина (внутривенно или внутримышечно), а также дозы и период лечения определяет лечащий врач. Инъекции внутримышечно малоэффективны по сравнению с уколами в вену. Они назначаются при болезнях средней тяжести. Внутривенные инъекции делают для быстрого улучшения состояния больного.
Актовегин для внутривенного введения назначают по 1 штуке в сутки, при этом доза может быть разной. Вливания препарата осуществляются струйно или капельно, что зависит от тяжести заболевания. Внутривенно струйно лекарство вливают в малом количестве стерильными шприцами, внутривенно капельно — в больших дозах с помощью капельниц. Капельное вливание проводится медленно — не более 2 мл за минуту.
В зависимости от курса лечения и тяжести клинической картины Актовегин внутривенно в первые дни вводят по 10-20 мл ежедневно, затем дозы сокращаются до 5-10 мл в день или нескольких уколов в неделю.
При дерматической или сосудистой терапии можно вводить Актовегин внутримышечно.
Выбирают место, на котором мышцы расположены вблизи кожного покрова — ягодицы, бедро или плечо.
Затем инъекционный участок обрабатывается антисептиком, вводится раствор с помощью шприца в количестве 5 мл внутримышечно. Для предотвращения появления сильного раздражающего эффекта ежедневную дозу для внутримышечного введения не увеличивают.
Уколы болючие, поэтому колоть внутримышечно нужно медленно.
Как разводить
Лекарственный препарат находится в готовом виде, его не надо смешивать с другими средствами или одновременно добавлять дополнительные компоненты. Иногда для детей инъекционный раствор смешивают с Новокаином, чтобы укол был менее болезненным.
При установлении капельниц делают разведенный раствор на основе 250-500 мл инфузии и 10-20 мл лекарства из ампул.
В какое время суток лучше колоть
Уколы разрешается колоть утром или вечером, на ночь перед сном.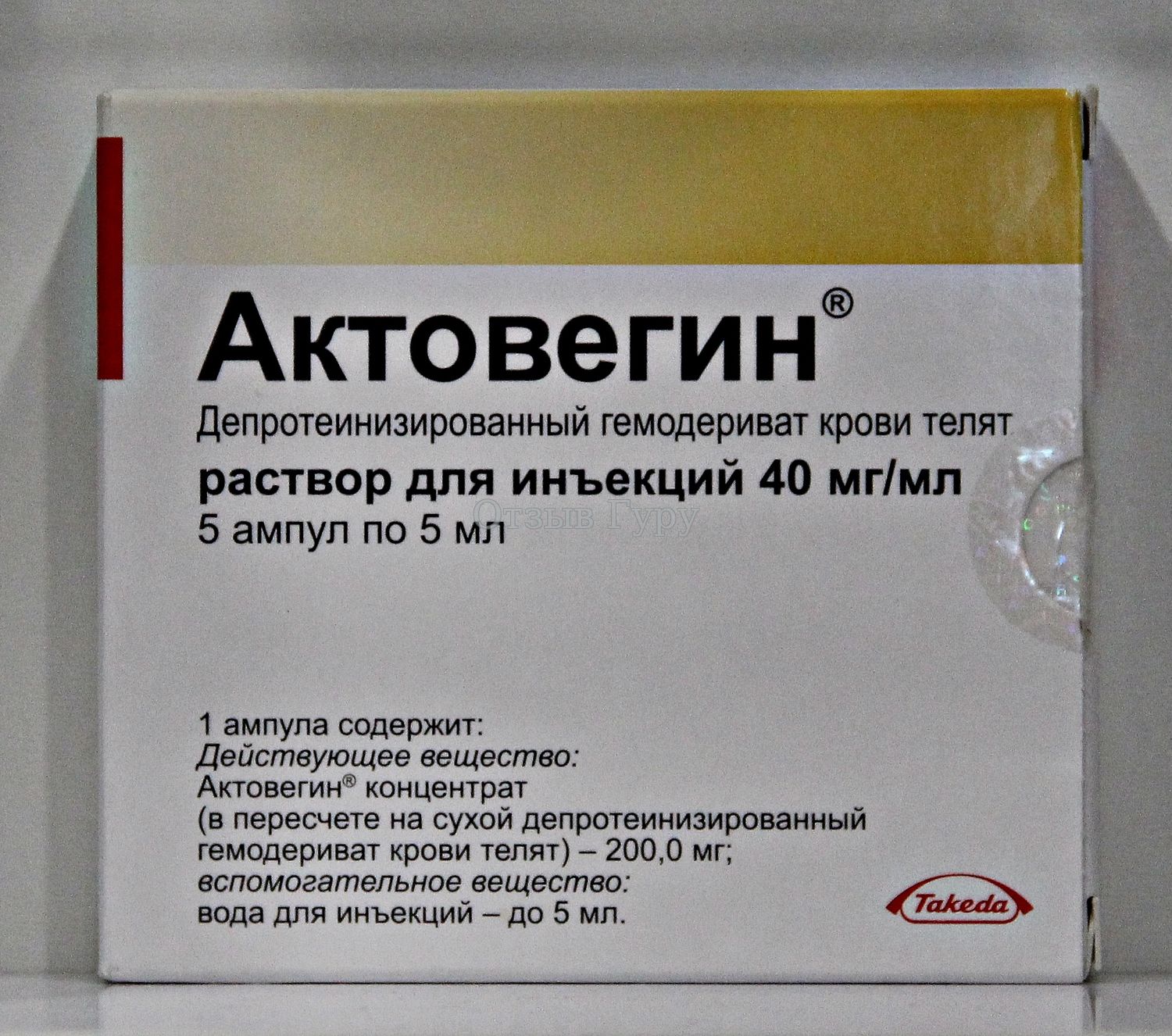
Сколько дней нужно колоть
Инъекционная терапия длится от 10 до 30 дней в зависимости от болезни и состояния больного.
Побочное действие
На основании медицинских исследований сделаны выводы о позитивном действии и хорошей переносимости Актовегина. Несмотря на это, уколы на основе гемодеривата и хлорида натрия способны вызвать разные побочные эффекты: от аллергических реакций в виде покраснения кожи, крапивницы, рвоты и повышения температуры тела до анафилактического шока.
Проявление боли в течение 20 минут не считается побочным действием и не может свидетельствовать о непереносимости лекарства. Если болезненные ощущения в голове, пояснице, суставах или месте укола не проходят, больной чувствует себя плохо, то следует своевременно обратиться к специалисту для отмены терапии данным препаратом и изменения курса лечения.
Взаимодействие с другими лекарственными средствами
Сведения о несовместимости раствора с другими медицинскими препаратами отсутствуют. Врачи при комплексной терапии разрешают делать уколы Комбилипеном и Актовегином. К Актовегину добавляют:
Врачи при комплексной терапии разрешают делать уколы Комбилипеном и Актовегином. К Актовегину добавляют:
- при болезнях головного мозга — Церебролизин;
- для лечения сосудистой патологии — Трентал.
Вместе с инъекционным раствором используют Мексидол. Их одновременно вводят внутримышечно разными шприцами.
Как хранить в ампулах
Ампулы должны находиться в специальной упаковке из картона, чтобы они не разбились. Во избежание попадания микробов и потери стерильности хранение ампул в разбитом или открытом состоянии не допускается; после вскрытия раствор требуется сразу использовать, при случайном вскрытии его уничтожают.
Условия хранения должны строго соблюдаться. Ампулы с раствором для инъекций помещают в защищенное от источника света, прохладное место. Температура окружающей среды не должна быть выше +25°С. Срок годности закрытых ампул составляет 3 года. По истечении этого времени лекарство использовать нельзя.
Температура окружающей среды не должна быть выше +25°С. Срок годности закрытых ампул составляет 3 года. По истечении этого времени лекарство использовать нельзя.
Актовегин — для чего назначают препарат? Применение в медицине
Актовегин — для чего назначают препарат? Применение в медицине
27 октября 2016 г.» Некоторые названия препаратов у всех на слуху. Не исключение и« Актовегин », для чего назначают и когда этот препарат применяют, знает большая часть населения. А несведущим читателям не помешает небольшое отступление. которые помогут восполнить этот пробел
Небольшой список возможных осложнений беременности.
Целевая аудитория продукта беременные. Эти прекрасные 40 недель для кого-то могут показаться адом, не все беременности одинаково хороши. Есть неприятные симптомы, в том числе:
- Постоянная тошнота, особенно по утрам.
- Стойкие изменения вкусовых предпочтений. Может подняться в страну желания поесть, извстку, щебнку
- Отек по всему телу, особенно поражаются нижние конечности. Это уже имеет место в анатомии и гемодинамике, особенно в крови.
- Общая слабость и недомогание. Часто сопровождается развитием депрессивных состояний и неустойчивого душевного состояния.
На самом деле список можно продолжать очень долго, с какими-то проблемами столкнется каждая женщина, только с другой «везет». Дело в том, что с момента оплодотворения у матери начинают происходить качественные и количественные изменения.
Только представьте, как сложно устроен человек. Организму беременной нужно 10 акушерских месяцев, чтобы в полной мере воспроизвести этот шедевр природы.
Для выполнения этой задачи мобилизуйте все внутренние ресурсы, иногда с матерью все еще слишком мало проблем в этом раздаче.
Можно ли рассчитывать на нормальное состояние здоровья беременной и отсутствие серьезных проявлений? Да хватит:
- Хорошая наследственность. Генетика играет огромную роль в развитии любых нарушений.
- Умение заниматься своим здоровьем.
- Достаточно свободного времени, чтобы расслабиться и не перегружать себя работой.
- Не мешайте, даже посетите женскую консультацию и получите консультацию врача. Но не все зависит от человека, на некоторые моменты мы никак не можем повлиять.
Если уже возникло состояние, требующее срочного медицинского вмешательства, лучше с этим не затягивать. Все продукты, предназначенные для беременных, проходят множество клинических исследований и всевозможных проверок, чтобы ученые могли гарантировать их качество. Штрафы, судебные иски, банкротство — в таком исходе не заинтересована ни одна компания.
Что принесет пользу беременным?
Чаще всего в списке приемов для беременных можно увидеть:
Восстановительная терапия:
- Витаминные препараты. Передержать сложно, но недостаток этих веществ может привести к серьезным отклонениям у ребенка. Особенно в развитии опорно-двигательного аппарата и нервной систем.
- Расслабляющий и лечебный массаж. В полном объеме это выполнить сложно или невозможно, но можно отвлечь внимание.
- Йодомарин с микро- и макроэлементами у беременной тоже бывает не так гладко. Поэтому необходимо назначать средства, помогающие восстановить метаболический баланс и исключить возможную патологию: как у матери, так и у новорожденного.
Специфические препараты:
- Кардиопротекторы — вещества, действующие на сердечную мышцу, снижающие риск сердечно-сосудистых патологий. Важный этап в подготовке беременной к родам.
- Актовегин . Благотворно влияет на кровеносную систему не только матери, но и плода. Его безопасность должна была проявиться в течение многих лет использования.
- Ангиотензин Лекарства. Повышенное артериальное давление по-прежнему остается серьезной проблемой для любого акушера. Специально разработанные для беременных средства оказывают более щадящее воздействие на весь организм. Ведь любой резкий перепад давления мог стать катастрофой для новой маленькой жизни. «Лабеталол» и «Метнулдопо» помогают справиться с гипертонией.
В каких случаях назначают «Актовегин»
На данный момент мы выяснили, что Актовегин назначают беременным. Осталось только выяснить, когда его могут назначить:
При невынашивании беременности в анамнезе. Предыдущие неблагоприятные исходы беременности не являются абсолютной мерой назначения препарата, но лучше перестраховаться. На этот раз трагедия не повторилась, и ничего не произошло.
- После осмотра «Доплера». Это исследование проводится в плановом порядке на поздних сроках беременности.По желанию пациента это может быть сделано на более раннем этапе, чтобы обеспечить нормальный кровоток. Если это не так — повод как можно быстрее начать прием соответствующих лекарств.
- По поводу скорости: также используется аварийный Актовегин. Правда внутривенно он уже введен, чтобы действовать быстрее и начал воздействовать уже в первые минуты после введения.
- При диагностике плацентарной недостаточности препарат выбора. Соединение системы матери и плода может иметь недостатки, возможные последствия, думаю, ясны.Именно через плаценту ребенок получает все необходимые питательные вещества.
Влияние Актовегина на организм беременной.
Основной механизм действия Актовегина связан с действием на эндотелиальные клетки сосудов. За счет воздействия веществ повышается их устойчивость к кислородному голоданию, что укрепляет структуру сосудистой стенки и улучшает некоторые возможности беременной женщины. Если в будущем случится непредвиденная ситуация, которая может привести к гипоксии плода, либо проблемы с кровообращением матери — организм будет к этому готов.
Кроме того, нормальное поглощение глюкозы клетками и другими питательными веществами из крови увеличивает их доставку в стенку сосуда. Причем здесь плацента? Оказалось, что как приятный бонус препарат положительно влияет на скорость и объем плацентарного кровотока.
Если в системе мать — плод есть патология, ее необходимо устранить. Для неотложной помощи Актовегин подходит в растворе в вену, если ситуация может быть пациентом, таблетки или капсулы. Побочные действия и противопоказания, как и у всех препаратов, но они незначительны.В основном занимаются аллергическими заболеваниями.
Нет необходимости назначать собственное лекарство или для профилактики, тем более для облегчения острых состояний. Сначала нужно обратиться к врачу, чтобы помощь была комплексной и эффективной.
Многие мамы рассказывают своим детям о препарате Актовегин, о том, что ему прописывают и как он спас жизнь когда-то маленькому. Статусу следует уделить должное внимание, особенно если речь идет о беременности.
Актовегин раствор для инъекций — DR.ДОПИНГ
Актовегин раствор для инъекций
19 июл 2018«Что такое Актовегин?»
«Как применять Актовегин?»
Такие вопросы задают нам читатели в своих письмах.
Актовегин — антигипоксическое средство, то есть препарат, улучшающий доставку кислорода к тканям. Благодаря способности повышать метаболизм в клетках тканей, последние эффективно поглощают глюкозу и кислород. Благодаря инъекциям Актовегина улучшается энергетика клетки, особенно при ишемии и гипоксии.Клинические исследования показали, что максимальный эффект Актовегина в ампулах наступает через 2-6 часов.
Актовегин в ампулах эффективен у пациентов с такими сопутствующими заболеваниями, как почечная или печеночная недостаточность. Также ампулы Актовегина применяют у пациентов пожилого возраста и новорожденных, у пациентов с сахарным диабетом 2 типа с диабетической полинейропатией. Актовегин применяется в неврологии, эндокринологии, кардиологии и др.
Актовегин в ампулах / Инструкция
Описание / Актовегин в ампулах
Раствор прозрачный в стеклянных ампулах.Слабый желтый раствор.
Состав / Актовегин в ампулах
Основное вещество: сухая депротеинизированная кровь телят. Вспомогательные компоненты: натрия хлорид, вода для инъекций, глюкоза безводная.
Показания к применению Актовегина в ампулах / Инструкция
1. Сосудистые и метаболические нарушения головного мозга (ишемический инсульт, церебральная недостаточность, энцефалопатия, черепно-мозговые травмы).
2. Заболевания периферических сосудов, а также их последствия.
Диабетическая полинейропатия, лучевая нейропатия, артериальная ангиопатия.
3. Актовегин в ампулах применяют при плохо заживающих ранах, а также в следующих случаях:
пролежнях, язвах различной этиологии, ожогах (химические и термические поражения нервной ткани, кожи, слизистых оболочек), лучевых поражениях. слизистые оболочки и кожа.
Противопоказания / Актовегин в ампулах
Индивидуальная аллергическая непереносимость инъекций Актовегина и аналогичных препаратов.Для инфузионных растворов — сердечная недостаточность в стадии декомпенсации, олигурия, отек легких, задержка жидкости в организме, анурия.
Для страдающих сахарным диабетом очень важно учитывать концентрацию глюкозы в растворе для инфузий Актовегина с декстрозой.
Способ применения Актовегина парентерально / Инструкция
Актовегин применяют внутривенно, внутримышечно или внутриартериально в ампулах по 10-20 мл или в виде инфузии с Актовегином, а затем — 5 мл внутривенно или внутримышечно ежедневно или несколько раз. неделя.В / м — вводить не более 5мл, т.к. раствор гипертонический.
При введении Актовегина в виде инфузий — 10-50 мл разводят в 200-300 мл натрия хлорида или 5% глюкозы.
Дозировка Актовегина в ампулах / Инструкция
Нарушения кровообращения и обмена веществ : первые инъекции Актовегина в / в ампулы по 10 мл ежедневно в течение двух недель, затем в / в 5-10 мл несколько раз в день в течение четырех недель.При ишемическом инсульте: 20-50 мл раствора Актовегина в 200-300 мл раствора основы, наносить ежедневно или несколько раз в течение двух-трех недель.
Артериальная ангиопатия : 20-50 мл Актовегина в 200-300 мл основного р-ра, в / в или в / в ежедневно или несколько раз в неделю (примерно, в течение четырех недель).
Ожоги различной этиологии : в / в в 10 мл Актовегина или в / м 5 мл Актовегина ежедневно или несколько раз в день.
Раствор Актовегина для в / в введения / Инструкция
Актовегин вводят от 250 мл в сутки в / в или в / в до 500 мл.Скорость ок. 2 мл / мин. Обычно назначают 10-20 инъекций Актовегина.
Нарушения обмена веществ и кровообращения головного мозга : внутривенно 250-500 мл / сут (в течение двух недель), затем по 250 мл несколько раз в неделю (не менее четырех недель).
Актовегин при ишемическом инсульте : в / в 250-500 мл Актовегина применяют ежедневно или несколько раз в неделю (в течение двух-трех недель).
Артериальная ангиопатия : в / в или 250 мл Актовегина ежедневно или несколько раз в неделю (четыре недели).
Актовегин при язвах, ожогах : в / в по 250 мл ежедневно или несколько раз в неделю.
Лучевое поражение кожи, слизистых оболочек : внутривенно 250 мл — за 1 день до начала лучевой терапии и две недели — после окончания терапии.
Дополнительная инструкция по применению Актовегина / Инструкция
1. При введении Актовегина в / м не превышайте дозу в 5 мл раствора, т.к. гипертонический (концентрированный).
2. Пробную реакцию Актовегина (2 мл раствора) обязательно проводить в связи с возможными анафилактическими реакциями.
3. Раствор Актовегина совместим с растворами натрия хлорида и 5% раствором глюкозы. Не рекомендуется смешивать с другими растворами.
Побочные действия Актовегина / Инструкция
Актовегин обычно хорошо переносится, редко возникают аллергические реакции, анафилактический шок.
Побочные эффекты Актовегина могут проявляться по-разному:
1.Со стороны иммунной системы: сыпь, зуд, гиперемия кожи, крапивница, повышенное потоотделение, отек слизистых оболочек и кожи, отек Квинке, озноб, повышение температуры тела.
2. Нервная система: головная боль, возбуждение, слабость, тремор, парестезии, обмороки.
3. Со стороны костно-мышечной системы: боли в суставах, пояснице, мышцах.
4. Пищеварительный тракт: боли в эпигастрии, диарея, тошнота, рвота.
5. Сердечно-сосудистая система: тахикардия, одышка, боли в области сердца, акроцианоз, артериальная гипертензия или гипотензия, бледность кожи.
6. Дыхательная система: приступ астмы, боль в горле, учащенное дыхание, затрудненное глотание, стеснение в груди.
7. Возможные реакции на месте введения Актовегина.
Актовегин при беременности и кормлении грудью
Применение препарата Актовегин при беременности только по назначению лечащего врача и под его контролем по жизненно важным показаниям (например, при патологической беременности, о которой также можно узнать Вот).
Дети: Актовегин, согласно инструкции, в педиатрии не применяется (из-за отсутствия доказательной базы). Но на практике Актовегин применяется в исключительных случаях (по жизненным показаниям).
Совместимость
Актовегин совместим с различными лекарственными средствами.
Управление транспортом с применением Актовегина
Исследования влияния Актовегина на скорость реакции при управлении автотранспортом не проводились.Однако следует учитывать возможность негативного воздействия Актовегина на нервную систему.
Передозировка : случаи передозировки Актовегина неизвестны.
Актовегин: Что это за фигня?
Вот что я нашел при быстром поиске в Google. Я видел это упомянуто в статье Тайгера Вудса как PED!Актовегин
Актовегин представляет собой депротеинизированное гемопроизводное телячьей крови, полученное с помощью ультрафильтрации. Депротеинизированное гемопроизводное крови теленка содержит только физиологические компоненты, неорганические вещества, такие как электролиты и незаменимые микроэлементы, и 30% органических компонентов, таких как аминокислоты, олигопептиды, нуклеозиды, промежуточные продукты метаболизма углеводов и жиров, а также компоненты клеточного мембраны в виде гликосфинголипидов.Одним из физиологических компонентов Актовегина являются фосфоолигосахариды инозитола (ИПО). Считается, что эти соединения обладают центральными и периферическими эффектами инсулина, что позволяет предположить, что терапевтический эффект может быть получен при нарушениях утилизации глюкозы. Молекулярная масса органических компонентов ниже 6000 Дальтон.
Фармакодинамика:
Активные компоненты в Актовегине способствуют захвату глюкозы церебральными и скелетными мышцами и другими клетками и стимулируют внутренний транспорт глюкозы, регулируя переносчик глюкозы GluT1; Актовегин активирует пируват-дегидрогеназу (ПДГ) и тем самым приводит к увеличению утилизации глюкозы клетками и образованию богатых энергией веществ («инсулиноподобный эффект»).(Oberermaier-Kusser et al. 1989 г. Актовегин также увеличивает поглощение и использование кислорода гипоксическими тканями и клетками (что может быть доказано тестом Варбурга) за счет стимулирования дыхательной функции митохондрий и уменьшения образования лактата, в результате он защищает гипоксическую ткань. (Машикао, 1993; Кунунака и др., 1991)
Токсикология:
Острая токсичность: Испытания на острую токсичность на мышах (мыши NMRI, смешанные самцы и самки) показали, что пятьдесят процентов летальных доз (LD50, рассчитанная как сухой вес) были следующими:
-внутреннее введение: 2.31 г / кг;
внутрибрюшинное введение: 2,97 г / кг;
-кожное введение: 5,57 г / кг;
— пероральное введение: 7,93 г / кг
Субхроническая токсичность: Эксперименты, проведенные на кроликах (кролики Deutsche Riesenschecken, самки), продемонстрировали отсутствие каких-либо макроскопических или микроскопических органических патологических изменений по сравнению с нормальными контрольными животными после внутривенного введения 20% Актовегина. 1 раз в сутки в дозе 7,0 мл / кг, 7 дней в неделю, в течение 3 месяцев.Актовегин не токсичен для фертильности, эмбриона и плода; не оказывает тератогенного, мутагенного или канцерогенного действия.
Фармакокинетика:
Актовегин — это гемодиализат, полученный из телячьей крови. Поскольку это не однокомпонентный препарат, проведение фармакокинетического исследования невозможно. Однако в отношении его биодоступности некоторые фармакологические исследования на животных могут дать некоторую справку: исследования толерантности к глюкозе на крысах показали, что уровень глюкозы в крови начал снижаться уже через 5 минут после внутривенного введения Актовегина, а эффект достиг своего пика через 180 минут. после администрации.(Bachmann et al. 1968) улучшилось через 15 минут после парентерального введения Актовегина. (Quadbeck et al. 1964)
Показания
Нарушения мозгового кровообращения и питания (ишемический инсульт, черепно-мозговые травмы).
Нарушения периферического (артериального, венозного) кровотока и последствия этих нарушений (артериальная ангиопатия, язвы).
Трансплантация кожи.
Ожоги, ожоги, эрозии.
Нарушения заживления ран: торпидные раны, пролежни;
Радиационно-индуцированные поражения кожи и слизистых оболочек (профилактика и терапия).
Принцип действия
Актовегин вызывает не связанное с органами повышение клеточного энергетического метаболизма. Активность подтверждается измерением повышенного поглощения и повышенного использования глюкозы и кислорода. Эти два эффекта взаимосвязаны и приводят к увеличению оборота АТФ и, таким образом, к большему обеспечению энергией в клетке. При дефицитных состояниях с нарушением нормальных функций энергетического обмена (гипоксия, дефицит субстрата) и при состояниях повышенной потребности в энергии (репарация, регенерация) Актовегин способствует энергозависимым процессам функционального метаболизма и метаболизма сохранения.Увеличение кровоснабжения рассматривается как вторичный эффект
Эффекты, связанные с терапевтическими показаниями:
Эффекты, связанные с транспортом глюкозы
-Фракция IPO Актовегина продемонстрировала положительный эффект на активность переносчика глюкозы (GLUT1) в плазматической мембране
-Актовегин стимулировал захват глюкозы тканями головного мозга, а также другими изолированными тканями животных
Эффекты, связанные с утилизацией глюкозы
-Фракция IPO Актовегина активировала окисление глюкозы, а также комплекс PHD
-Фракция IPO Актовегина косвенно влияет на цикл лимонной кислоты, вызывая повышенное образование ацетил-COA
.
Влияние потребления кислорода на энергетический обмен
-Актовегин увеличивал дыхательную способность митохондрий
-Актовегин улучшил потребление кислорода у собак под наркозом
-Актовегин продемонстрировал положительное влияние на церебральный метаболизм крыс в условиях гипоксии
Безопасность Актовегина
Производитель Nycomed Austria GmbH подтверждает, что приняты все меры, гарантирующие безопасность Актовегина TSE.Согласно действующему руководству EMEA / 410/01 final (выпущенному в феврале 2001 г., заменяющему CPMP / BWP / 1230 REV.1) и Заключительному заключению Научного руководящего комитета по географическому риску BSE (выпущенному в июле 200 г.) безопасность лекарственный препарат определяется несколькими важными факторами:
1. Животные как источник материала: наиболее удовлетворительный источник материалов — из стран, свободных от BSE и имеющих соответствующие системы надзора. Могут использоваться материалы из стран с низкой заболеваемостью BSE.Кровь телят, используемая в качестве сырья для Актовегина, происходит от телят, рожденных, выращенных и забитых в Австралии. Австралия официально признана страной, свободной от коровьего бешенства и скрепи, МЭБ (Всемирная организация здоровья животных) и SSC (Научный руководящий комитет Европейского союза). Существуют системы наблюдения.
2. Части тел животных и биологические жидкости, используемые в качестве исходных материалов: ткани и биологические жидкости подразделяются на четыре категории (от категории I = высокая инфекционность, такая как мозг, до категории IV = самая безопасная категория, не обнаруживаемая инфекционность, такая как кровь и молоко).Актовегин производится из крови теленка, кровь относится к IV категории наиболее безопасных тканей.
3. Возраст животных: получение молодняка считается очень важным фактором безопасности. Кровь, используемая в качестве сырья для производства Актовегина, происходит от телят младше шести месяцев. Телята никогда не получали корма из туш животных и признаны годными для употребления в пищу, что подтверждается ветеринарными сертификатами. Кроме того, обеспечивается отслеживаемость каждой партии Актовегина до отдельных телят как доноров крови.Известны также коровы-матери (матери) телят.
4. Производственный процесс должен быть разработан таким образом, чтобы удалять или инактивировать агенты TSE. В настоящее время валидационные исследования обычно не требуются. Процесс производства Актовегина утвержден на ГЭКРС, что доказывает его способность удалять гипотетически присутствующие агенты TSE.
5. Анализ рисков был проведен в соответствии с системой PhPMA, показывающий, что Актовегин абсолютно безопасен в отношении коровьего бешенства. Более того, Актовегин — это натуральный препарат с доказанной эффективностью и общим благоприятным профилем безопасности на протяжении десятилетий.Эти преимущества нельзя заменить химическим препаратом. В заключение, Актовегин безопасен для коровьего бешенства и обеспечивает даже больше мер безопасности, чем того требуют действующие нормы.
Размеры упаковки
400 мг / 10 мл 5
Срок годности
60 месяцев
http://www.nycomed.com.cn/english/wmdcp/awz/biaoti.html
Информация о назначении FDA, побочные эффекты и способы применения
Общее название: тоцилизумаб
Лекарственная форма: раствор для инъекций, концентрат
Медицинское заключение компании Drugs.com. Последнее обновление: 1 июня 2020 г.
ВНИМАНИЕ: РИСК СЕРЬЕЗНЫХ ИНФЕКЦИЙПациенты, получавшие Actemra, подвергаются повышенному риску развития серьезных инфекций, которые могут привести к госпитализации или смерти [см. Предупреждения и меры предосторожности (5.1), Побочные реакции (6.1)]. Большинство пациентов, у которых развились эти инфекции, принимали сопутствующие иммунодепрессанты, такие как метотрексат или кортикостероиды.
Если развивается серьезная инфекция, прервите прием Актемры до тех пор, пока инфекция не пройдет.
Зарегистрированные инфекции:
- Активный туберкулез, который может проявляться легочной или внелегочной болезнью. Перед применением Актемры и во время терапии пациенты должны пройти обследование на латентный туберкулез. Перед применением Актемры следует начать лечение скрытой инфекции.
- Инвазивные грибковые инфекции, включая кандидоз, аспергиллез и пневмоцист. Пациенты с инвазивными грибковыми инфекциями могут иметь диссеминированное, а не локализованное заболевание.
- Бактериальные, вирусные и другие инфекции, вызванные условно-патогенными микроорганизмами.
Риски и преимущества лечения препаратом Актемра следует тщательно рассмотреть до начала терапии у пациентов с хронической или рецидивирующей инфекцией.
Пациенты должны находиться под тщательным наблюдением на предмет развития признаков и симптомов инфекции во время и после лечения препаратом Актемра, включая возможное развитие туберкулеза у пациентов с отрицательным результатом на латентную туберкулезную инфекцию до начала терапии [см. Предупреждения и меры предосторожности (5.1)].
Показания и использование для Actemra
Ревматоидный артрит (РА)
Актемра® (тоцилизумаб) показан для лечения взрослых пациентов с умеренно или сильно активным ревматоидным артритом, у которых был неадекватный ответ на один или несколько модифицирующих болезнь антиревматических препаратов (DMARD).
Гигантоклеточный артериит (GCA)
Актемра® (тоцилизумаб) показан для лечения гигантоклеточного артериита (ГКА) у взрослых пациентов.
Полиартикулярный юношеский идиопатический артрит (ПЮИА)
Актемра® (тоцилизумаб) показан для лечения активного полиартикулярного ювенильного идиопатического артрита у пациентов в возрасте 2 лет и старше.
Системный ювенильный идиопатический артрит (СЮИА)
Актемра® (тоцилизумаб) показан для лечения активного системного ювенильного идиопатического артрита у пациентов в возрасте 2 лет и старше.
Синдром высвобождения цитокинов (CRS)
Актемра® (тоцилизумаб) показан для лечения индуцированного химерными рецепторами антигена (CAR) Т-лимфоцитов тяжелого или опасного для жизни синдрома высвобождения цитокинов у взрослых и детей в возрасте 2 лет и старше.
Администрация и дозировка Actemra
Ревматоидный артрит
Актемра может использоваться в качестве монотерапии или одновременно с метотрексатом или другими небиологическими БПВП в виде внутривенной инфузии или подкожной инъекции.
Рекомендуемый режим внутривенной дозировки:
Рекомендуемая доза Актемры для взрослых пациентов, вводимых в виде 60-минутной однократной внутривенной капельной инфузии, составляет 4 мг на кг каждые 4 недели с последующим увеличением до 8 мг на кг каждые 4 недели в зависимости от клинического ответа.
Рекомендуемый режим подкожной дозировки:
| Пациенты весом менее 100 кг | 162 мг вводят подкожно каждые две недели с последующим повышением дозы каждую неделю в зависимости от клинического ответа |
| Пациенты с массой тела 100 кг и более | 162 мг вводить подкожно каждую неделю |
При переходе от внутривенной терапии Актемрой к подкожному введению вводят первую подкожную дозу вместо следующей запланированной внутривенной дозы.
Прерывание дозы или уменьшение частоты введения подкожной дозы с каждой недели на каждую вторую неделю рекомендуется для управления определенными дозозависимыми лабораторными изменениями, включая повышение ферментов печени, нейтропению и тромбоцитопению [см. Дозировка и администрация (2.9), Предупреждения и меры предосторожности (5.3, 5.4) и побочные реакции (6.2)].
Гигантоклеточный артериит
Рекомендуемая доза Актемры для взрослых пациентов с ГКА составляет 162 мг один раз в неделю в виде подкожной инъекции в сочетании с постепенным курсом глюкокортикоидов.
Доза 162 мг, вводимая один раз в две недели в виде подкожной инъекции в сочетании с постепенным курсом глюкокортикоидов, может быть назначена на основании клинических соображений.
Актемра можно использовать отдельно после прекращения приема глюкокортикоидов.
- Прерывание дозирования может потребоваться для управления дозозависимыми лабораторными отклонениями, включая повышенные ферменты печени, нейтропению и тромбоцитопению [см. Дозировка и управление (2.9)].
- Внутривенное введение не одобрено для GCA.
Полиартикулярный ювенильный идиопатический артрит
Actemra можно использовать в виде внутривенной инфузии или подкожной инъекции отдельно или в комбинации с метотрексатом. Не изменяйте дозу только на основании измерения веса тела за одно посещение, так как вес может колебаться.
Рекомендуемый режим внутривенной дозировки:
Рекомендуемая доза Актемры для пациентов с ПЮИА, вводимых один раз в 4 недели в виде 60-минутной однократной внутривенной капельной инфузии, составляет:
| Рекомендуемая внутривенная дозировка PJIA каждые 4 недели | |
|---|---|
| Пациенты с массой тела менее 30 кг | 10 мг на кг |
| Пациенты с массой тела 30 кг и более | 8 мг на кг |
Рекомендуемый режим подкожной дозировки:
| Рекомендуемая дозировка для подкожного ПЮИА | |
|---|---|
| Пациенты с массой тела менее 30 кг | 162 мг 1 раз в 3 недели |
| Пациенты с массой тела 30 кг и более | 162 мг 1 раз в 2 недели |
При переходе от внутривенной терапии Актемрой к подкожному введению введите первую подкожную дозу вместо следующей запланированной внутривенной дозы.
Прерывание дозирования может потребоваться для управления дозозависимыми лабораторными отклонениями, включая повышенные ферменты печени, нейтропению и тромбоцитопению [см. Дозировка и управление (2.9)].
Системный ювенильный идиопатический артрит
Actemra можно использовать в виде внутривенной инфузии или подкожной инъекции отдельно или в комбинации с метотрексатом. Не изменяйте дозу только на основании измерения веса тела за одно посещение, так как вес может колебаться.
Рекомендуемый режим внутривенной дозировки:
Рекомендуемая доза Актемры для пациентов с сЮИА, вводимых один раз в 2 недели в виде 60-минутной однократной внутривенной капельной инфузии:
| Рекомендуемая внутривенная дозировка SJIA каждые 2 недели | |
|---|---|
| Пациенты с массой тела менее 30 кг | 12 мг на кг |
| Пациенты с массой тела 30 кг и более | 8 мг на кг |
Рекомендуемый режим подкожной дозировки:
| Рекомендуемая дозировка SJIA для подкожного введения | |
|---|---|
| Пациенты с массой тела менее 30 кг | 162 мг один раз в две недели |
| Пациенты с массой тела 30 кг и более | 162 мг один раз в неделю |
При переходе от внутривенной терапии Актемрой к подкожному введению вводите первую подкожную дозу, когда наступает срок следующей запланированной внутривенной дозы.
Прерывание дозирования может потребоваться для управления дозозависимыми лабораторными отклонениями, включая повышенные ферменты печени, нейтропению и тромбоцитопению [см. Дозировка и управление (2.9)].
Синдром высвобождения цитокинов (CRS)
Используйте только внутривенный путь для лечения СВК. Рекомендуемая доза Актемры для лечения СВК в виде 60-минутной внутривенной инфузии составляет:
| Рекомендуемая внутривенная дозировка CRS | |
|---|---|
| Пациенты с массой тела менее 30 кг | 12 мг на кг |
| Пациенты с массой тела 30 кг и более | 8 мг на кг |
| Самостоятельно или в сочетании с кортикостероидами | |
- Если после первой дозы клинического улучшения признаков и симптомов СВК не происходит, можно ввести до 3 дополнительных доз Актемры.Интервал между последовательными приемами должен составлять не менее 8 часов.
- Дозы, превышающие 800 мг на инфузию, не рекомендуются пациентам с СВК.
- Подкожное введение не одобрено для CRS
Общие рекомендации по администрированию
- Actemra не изучалась в сочетании с биологическими DMARD, такими как антагонисты TNF, антагонисты IL-1R, моноклональные антитела против CD20 и селективные модуляторы костимуляции из-за возможности повышенной иммуносупрессии и повышенного риска инфекции.Избегайте использования Actemra с биологическими DMARD.
- Не рекомендуется назначать препарат Актемра пациентам с абсолютным числом нейтрофилов (АНК) ниже 2000 на мм3, числом тромбоцитов ниже 100000 на мм3 или у которых уровень АЛТ или АСТ в 1,5 раза превышает верхний предел нормы (ВГН).
- —
- Пациенты с тяжелым или опасным для жизни СВК часто имеют цитопению или повышенный уровень АЛТ или АСТ из-за лимфодеплецирующей химиотерапии или СВК. Решение о применении Актемры должно учитывать потенциальную пользу лечения СВК по сравнению с рисками краткосрочного лечения Актемрой.
Инструкции по приготовлению и применению для внутривенной инфузии
Актемра для внутривенного вливания должен быть разбавлен медицинским работником в асептических условиях следующим образом:
- Пациенты с массой тела менее 30 кг: используйте инфузионный пакет на 50 мл или бутылку с 0,9% или 0,45% раствором хлорида натрия для инъекций, USP, а затем выполните шаги 1 и 2 ниже.
- Пациенты с массой тела 30 кг и более: воспользуйтесь пакетом или бутылкой для инфузии на 100 мл, а затем выполните шаги 1 и 2 ниже.
- —
- Шаг 1. Из инфузионного мешка или бутылки извлеките объем 0,9% или 0,45% раствора хлорида натрия, USP, равный объему инъекции Actemra, необходимому для дозы пациента [см. Дозировка и администрация (2.1, 2.3, 2.4, 2.5)].
| Для внутривенного использования: объем инъекции Актемры на кг массы тела | ||
|---|---|---|
| Дозировка | Индикация | Объем инъекции Актемры на кг массы тела |
| 4 мг / кг | Взрослый RA | 0.2 мл / кг |
| 8 мг / кг | RA для взрослых SJIA, PJIA и CRS (масса тела превышает или равна 30 кг) | 0,4 мл / кг |
| 10 мг / кг | PJIA (масса тела менее 30 кг) | 0,5 мл / кг |
| 12 мг / кг | ЮИА и СВК (масса тела менее 30 кг) | 0,6 мл / кг |
- —
- Шаг 2. Выньте количество Актемры для внутривенной инфузии из флакона (флаконов) и медленно добавьте в 0.Раствор для инъекций 9% или 0,45% хлорида натрия, пакет для инфузии USP или бутылка. Чтобы перемешать раствор, осторожно переверните пакет, чтобы не допустить вспенивания.
- Полностью разбавленные растворы Actemra для инфузий с использованием 0,9% раствора хлорида натрия, USP, могут храниться при температуре от 2 ° до 8 ° C (от 36 ° до 46 ° F) или комнатной температуре в течение до 24 часов и должны быть защищены от света. .
- Полностью разбавленные растворы Actemra для инфузий с использованием 0,45% раствора хлорида натрия для инъекций, USP, могут храниться при температуре от 2 до 8 ° C (от 36 до 46 ° F) до 24 часов или при комнатной температуре до 4 часов и должны храниться защищен от света.
- Растворы Актемры не содержат консервантов; поэтому неиспользованный продукт, оставшийся во флаконах, использовать нельзя.
- Перед инфузией дайте полностью разбавленному раствору Actemra достичь комнатной температуры.
- Настой следует вводить в течение 60 минут с помощью набора для инфузии. Не вводить внутривенно или болюсно.
- Актемра не следует вводить одновременно с другими лекарственными препаратами в одной внутривенной линии.Никаких исследований физической или биохимической совместимости для оценки одновременного применения Актемры с другими лекарственными средствами не проводилось.
- Лекарственные препараты для парентерального введения следует проверять визуально на предмет наличия твердых частиц и обесцвечивания перед введением, если позволяют раствор и контейнер. Если отмечены частицы и изменение цвета, продукт не следует использовать.
- Полностью разбавленные растворы Actemra совместимы с инфузионными пакетами из полипропилена, полиэтилена и поливинилхлорида, а также с полипропиленовыми, полиэтиленовыми и стеклянными инфузионными бутылками.
Инструкции по приготовлению и введению подкожной инъекции
- Актемра для подкожного введения не предназначена для внутривенного капельного введения.
- Оцените пригодность пациента для подкожного домашнего использования и проинструктируйте пациентов проинформировать медицинского работника перед введением следующей дозы, если у них возникнут какие-либо симптомы аллергической реакции. Пациентам следует немедленно обратиться за медицинской помощью, если у них появятся симптомы серьезных аллергических реакций.Подкожная инъекция Actemra предназначена для использования под наблюдением врача. После надлежащего обучения технике подкожных инъекций пациент может самостоятельно вводить Актемру, или лицо, ухаживающее за пациентом, может вводить Актемру, если практикующий врач сочтет это целесообразным. Пациенты с PJIA и SJIA могут самостоятельно вводить инъекции с помощью предварительно заполненного шприца Actemra или автоинжектора ACTPen®, или лицо, осуществляющее уход за пациентом, может вводить Actemra, если и практикующий врач, и родитель / законный опекун сочтут это целесообразным [см. Использование в конкретных группах населения (8.4)]. Пациенты или лица, ухаживающие за ними, должны быть проинструктированы следовать указаниям, приведенным в Инструкциях по применению (IFU) для получения дополнительных сведений о приеме лекарств.
- Лекарственные препараты для парентерального введения следует проверять визуально на наличие твердых частиц и обесцвечивания перед введением. Не используйте предварительно заполненные шприцы (PFS) Actemra или предварительно заполненные автоинжекторы ACTPen®, имеющие твердые частицы, помутнение или изменение цвета. Актемра для подкожного введения должна быть прозрачной от бесцветной до бледно-желтой.Не используйте, если какая-либо часть автоинжектора PFS или ACTPen® повреждена.
- Пациенты, использующие Актемру для подкожного введения, должны быть проинструктированы вводить полное количество шприцом (0,9 мл) или полное количество в автоинжектор ACTPen® (0,9 мл), который обеспечивает 162 мг Актемры, в соответствии с инструкциями, приведенными в инструкции по применению. .
- Места инъекций следует менять при каждой инъекции и никогда не следует вводить в родинки, шрамы или участки, где кожа нежная, с синяками, красная, твердая или поврежденная.
Изменения дозировки в связи с серьезными инфекциями или лабораторными отклонениями
Прекратите лечение Актемрой, если у пациента разовьется серьезная инфекция, пока инфекция не будет куплена.
Ревматоидный артрит и гигантоклеточный артериит
| Нарушения ферментов печени [см. Предупреждения и меры предосторожности (5.3,5.4)]: | |
|---|---|
| Лабораторное значение | Рекомендация |
| От 1 до 3 × ULN | Изменение дозы сопутствующего DMARD (RA) или иммуномодулирующих агентов (GCA), если необходимо. Для стойкого повышения в этом диапазоне:
|
| От 3 до 5 × ULN (подтверждено повторными испытаниями) | Удерживайте дозировку Actemra до тех пор, пока не будет меньше 3 × ULN, и следуйте рекомендациям выше для более чем 1–3 × ULN При стойком увеличении более чем 3 × ULN прекратите прием Actemra |
| Более 5 × ULN | Прекратить производство Actemra |
| Низкое абсолютное количество нейтрофилов (ANC) [см. Предупреждения и меры предосторожности (5.4)]: | |
|---|---|
| Лабораторное значение (клеток на мм3) | Рекомендация |
| ANC больше 1000 | Поддерживать дозу |
| ANC от 500 до 1000 | Удерживайте дозировку Actemra Когда ANC превышает 1000 клеток на мм3:
|
| ANC менее 500 | Прекратить производство Actemra |
| Низкое количество тромбоцитов [см. Предупреждения и меры предосторожности (5.4)]: | |
|---|---|
| Лабораторное значение (клеток на мм3) | Рекомендация |
| от 50 000 до 100 000 | Hold Actemra dosing Когда количество тромбоцитов превышает 100 000 клеток на мм3:
|
| Менее 50 000 | Прекратить производство Actemra |
Полиартикулярный и системный ювенильный идиопатический артрит:
Снижение дозы Actemra не изучалось в популяциях PJIA и SJIA.Прекращение приема препарата Актемра рекомендуется при нарушениях ферментов печени, низком количестве нейтрофилов и низком количестве тромбоцитов у пациентов с ПЮИА и сЮИА на уровнях, аналогичных указанным выше для пациентов с РА и ГКА. При необходимости измените дозу или отмените сопутствующий прием метотрексата и / или других лекарств и удерживайте прием Актемры до тех пор, пока не будет оценена клиническая ситуация. При ПЮИА и СЮИА решение о прекращении приема препарата Актемра из-за лабораторных отклонений должно основываться на медицинской оценке конкретного пациента.
Лекарственные формы и сила действия
Внутривенное вливание
Раствор для инъекций: 80 мг / 4 мл, 200 мг / 10 мл, 400 мг / 20 мл в виде прозрачного раствора от бесцветного до бледно-желтого цвета во флаконах для однократной дозы 20 мг / мл для дальнейшего разбавления перед внутривенной инфузией.
Подкожная инъекция
Раствор для инъекций: 162 мг / 0,9 мл прозрачный раствор от бесцветного до слегка желтоватого цвета в предварительно заполненном однократном шприце или предварительно заполненном однократном дозе ACTPen® автоинъекторе.
Противопоказания
Actemra противопоказан пациентам с известной гиперчувствительностью к Actemra [см. Предупреждения и меры предосторожности (5.6)].
Предупреждения и меры предосторожности
Серьезные инфекции
Сообщалось о серьезных и иногда смертельных инфекциях, вызванных бактериальными, микобактериальными, инвазивными грибковыми, вирусными, протозойными или другими условно-патогенными микроорганизмами у пациентов, получающих иммунодепрессанты, включая Actemra. Наиболее распространенные серьезные инфекции включали пневмонию, инфекцию мочевыводящих путей, целлюлит, опоясывающий герпес, гастроэнтерит, дивертикулит, сепсис и бактериальный артрит [см. Побочные реакции (6.1)]. Среди оппортунистических инфекций при приеме Актемры были зарегистрированы туберкулез, криптококк, аспергиллез, кандидоз и пневмоцистоз. Также могут возникать другие серьезные инфекции, о которых не сообщалось в клинических исследованиях (например, гистоплазмоз, кокцидиоидомикоз, листериоз). Пациенты имели диссеминированное, а не локализованное заболевание, и часто принимали сопутствующие иммунодепрессанты, такие как метотрексат или кортикостероиды, которые в дополнение к ревматоидному артриту могут предрасполагать их к инфекциям.
Не применяйте Актемру пациентам с активной инфекцией, включая локализованные инфекции. Перед назначением препарата Актемра пациентам следует учитывать риски и преимущества лечения:
- с хронической или рецидивирующей инфекцией;
- человек, заболевших туберкулезом;
- с историей серьезной или оппортунистической инфекции;
- , которые проживали или путешествовали в районах, пораженных эндемическим туберкулезом или эндемическими микозами; или
- с сопутствующими заболеваниями, которые могут предрасполагать их к инфекции.
Внимательно следить за пациентами на предмет развития признаков и симптомов инфекции во время и после лечения препаратом Актемра, поскольку признаки и симптомы острого воспаления могут быть уменьшены из-за подавления реактантов острой фазы [см. Дозировка и администрация (2.6), Побочные реакции (6.1) и информация для консультирования пациентов (17)].
Удерживайте Actemra, если у пациента развивается серьезная инфекция, оппортунистическая инфекция или сепсис. Пациент, у которого развивается новая инфекция во время лечения Актемрой, должен пройти быстрое и полное диагностическое обследование, соответствующее пациенту с ослабленным иммунитетом, начать соответствующую противомикробную терапию и внимательно наблюдать за пациентом.
Туберкулез
Обследуйте пациентов на наличие факторов риска туберкулеза и исследуйте латентную инфекцию до начала приема препарата Актемра.
Рассмотреть противотуберкулезную терапию до начала применения Актемры у пациентов с анамнезом латентного или активного туберкулеза, у которых нельзя подтвердить адекватный курс лечения, и у пациентов с отрицательным тестом на латентный туберкулез, но имеющих факторы риска туберкулезной инфекции . Рекомендуется проконсультироваться с врачом, имеющим опыт лечения туберкулеза, чтобы принять решение о целесообразности начала противотуберкулезной терапии для конкретного пациента.
Внимательно следите за пациентами на предмет развития признаков и симптомов туберкулеза, включая пациентов с отрицательными результатами тестов на латентную туберкулезную инфекцию, до начала лечения.
Перед началом приема препарата Актемра рекомендуется обследовать пациентов на наличие скрытой туберкулезной инфекции. Заболеваемость туберкулезом в мировых программах клинической разработки составляет 0,1%. Пациенты с латентным туберкулезом должны пройти стандартную антимикобактериальную терапию до начала приема препарата Актемра.
Вирусная реактивация
Сообщалось о реактивации вируса при иммуносупрессивной биологической терапии, а в клинических исследованиях с Actemra наблюдались случаи обострения опоясывающего герпеса. Случаев реактивации гепатита B в ходе испытаний не наблюдалось; однако пациенты с положительным результатом скрининга на гепатит были исключены.
Перфорация желудочно-кишечного тракта
Случаи перфорации желудочно-кишечного тракта были зарегистрированы в клинических испытаниях, прежде всего как осложнения дивертикулита у пациентов, получавших Актемру.Актемра следует применять с осторожностью у пациентов, которые могут подвергаться повышенному риску перфорации желудочно-кишечного тракта. Своевременно оцените пациентов с новыми абдоминальными симптомами для раннего выявления перфорации желудочно-кишечного тракта [см. Побочные реакции (6.1)].
Гепатотоксичность
Серьезные случаи повреждения печени наблюдались у пациентов, принимавших Актемру внутривенно или подкожно. Некоторые из этих случаев закончились трансплантацией печени или смертью. Время до начала заболевания варьировало от месяцев до лет после начала лечения тоцилизумабом.В то время как в большинстве случаев наблюдалось заметное повышение уровня трансаминаз (> 5 раз ULN), в некоторых случаях наблюдались признаки или симптомы дисфункции печени и лишь незначительное повышение уровня трансаминаз.
Во время рандомизированных контролируемых исследований лечение Actemra было связано с более высокой частотой повышения трансаминаз [см. Побочные реакции (6.1, 6.2, 6.4, 6.6)]. Повышенная частота и величина этих повышений наблюдались при использовании потенциально гепатотоксичных препаратов (например, метотрексата) в сочетании с Актемрой.
Для пациентов с RA и GCA получите панель тестов печени (сывороточная аланинаминотрансфераза [ALT], аспартатаминотрансфераза [AST], щелочная фосфатаза и общий билирубин) перед началом лечения Actemra, каждые 4-8 недель после начала терапии в течение первых шести недель. месяцев лечения и каждые 3 месяца в дальнейшем. Не рекомендуется начинать лечение Актемрой у пациентов с РА или ГКА с повышенным уровнем трансаминаз АЛТ или АСТ, превышающим 1,5 × ВГН. У пациентов, у которых наблюдается повышенный уровень АЛТ или АСТ, превышающий 5 × ULN, прекратите прием Актемры.Рекомендуемые модификации, основанные на увеличении трансаминаз, см. В разделе «Дозировка и администрация» (2.9).
Оперативно измеряйте пробы печени у пациентов, которые сообщают о симптомах, которые могут указывать на повреждение печени, таких как усталость, анорексия, дискомфорт в правом верхнем углу живота, темная моча или желтуха. В этом клиническом контексте, если у пациента обнаруживаются отклонения от нормы печеночных тестов (например, уровень АЛТ более чем в три раза превышает верхний предел референсного диапазона, общий билирубин в сыворотке более чем в два раза превышает верхний предел референсного диапазона), лечение Актемрой следует быть прервано и проведено расследование для установления вероятной причины.Актемру следует возобновлять только пациентам с другим объяснением отклонений печеночных пробы после их нормализации.
Аналогичная картина повышения уровня печеночных ферментов отмечается при лечении Актемрой в популяциях PJIA и SJIA. Контролируйте панель печеночного теста во время второго введения, а затем каждые 4-8 недель для PJIA и каждые 2-4 недели для SJIA.
Параметры лаборатории
Ревматоидный артрит и гигантоклеточный артериит
Нейтропения
Лечение Актемрой было связано с более высокой частотой нейтропении.В долгосрочных расширенных исследованиях и постмаркетинговом клиническом опыте редко сообщалось об инфекциях, связанных с нейтропенией, связанной с лечением.
- —
- Не рекомендуется начинать лечение Актемрой у пациентов с низким числом нейтрофилов, т. Е. Абсолютным числом нейтрофилов (АНК) менее 2000 на мм3. Пациентам, у которых абсолютное количество нейтрофилов ниже 500 на мм3, лечение не рекомендуется.
- –
- Контролируйте нейтрофилы через 4-8 недель после начала терапии и каждые 3 месяца после этого [см. Клиническая фармакология (12.2)]. Рекомендуемые модификации, основанные на результатах АНК, см. В разделе «Дозировка и администрация» (2.9).
Тромбоцитопения
Лечение Actemra было связано со снижением количества тромбоцитов. Связанное с лечением снижение тромбоцитов не было связано с серьезными кровотечениями в клинических испытаниях [см. Побочные реакции (6.1, 6.2)].
- —
- Не рекомендуется начинать лечение Актемрой у пациентов с количеством тромбоцитов ниже 100 000 на мм3.Пациентам, у которых количество тромбоцитов ниже 50 000 на мм3, лечение не рекомендуется.
- –
- Мониторинг тромбоцитов через 4-8 недель после начала терапии и каждые 3 месяца после этого. Рекомендуемые модификации на основе количества тромбоцитов см. В разделе «Дозировка и администрация» (2.9).
Повышенные ферменты печени
См. 5.3 Гепатотоксичность. Для рекомендуемых модификаций [см. Дозировка модификации 2.9]
Нарушения липидов
Лечение Actemra было связано с увеличением липидных параметров, таких как общий холестерин, триглицериды, холестерин ЛПНП и / или холестерин ЛПВП [см. Побочные реакции (6.1, 6.2)].
- —
- Оцените параметры липидов примерно через 4-8 недель после начала терапии Actemra.
- –
- Затем ведите пациентов в соответствии с клиническими рекомендациями [например, Национальной образовательной программой по холестерину (NCEP)] для лечения гиперлипидемии.
Полиартикулярный и системный ювенильный идиопатический артрит
Аналогичная картина повышения уровня печеночных ферментов, низкого количества нейтрофилов, низкого количества тромбоцитов и повышения липидов отмечается при лечении Актемрой в популяциях PJIA и SJIA.Контролируйте нейтрофилы, тромбоциты, АЛТ и АСТ во время второго введения, а затем каждые 4–8 недель для PJIA и каждые 2–4 недели для SJIA. Следите за липидами, как указано выше для утвержденных показаний для взрослых [см. Администрация и дозировка (2.9)].
Иммуносупрессия
Влияние лечения с Actemra на развитие злокачественных новообразований не известно, но злокачественные новообразования наблюдались в клинических исследованиях [см. Побочные реакции (6.1)]. Актемра является иммунодепрессантом, и лечение иммунодепрессантами может привести к повышенному риску злокачественных новообразований.
Реакции гиперчувствительности, включая анафилаксию
Сообщалось ореакциях гиперчувствительности, включая анафилаксию, в связи с Actemra [см. Побочные реакции (6)] и анафилактических событиях с летальным исходом с внутривенным вливанием Actemra. Анафилаксия и другие реакции гиперчувствительности, потребовавшие прекращения лечения, были зарегистрированы у 0,1% (3 из 2644) пациентов в 6-месячных контролируемых испытаниях внутривенного введения Актемры, 0.2% (8 из 4009) пациентов в популяции внутривенного РА с полным воздействием, 0,7% (8 из 1068) в исследованиях подкожного 6-месячного контролируемого РА и 0,7% (10 из 1465) пациентов в подкожная популяция, подверженная всем воздействиям. В контролируемом исследовании SJIA с внутривенным введением Актемры у 1 из 112 пациентов (0,9%) наблюдались реакции гиперчувствительности, требовавшие прекращения лечения. В контролируемом исследовании PJIA с внутривенным введением Actemra 0 из 188 пациентов (0%) в популяции Actemra, получавшей все воздействие, испытали реакции гиперчувствительности, которые потребовали прекращения лечения.Реакции, потребовавшие прекращения лечения, включали генерализованную эритему, сыпь и крапивницу. Реакции сайта инъекции были классифицированы отдельно [см. Побочные реакции (6)].
В условиях постмаркетинга события реакции гиперчувствительности, включая анафилаксию и смерть, произошли у пациентов, получавших ряд доз Актемры внутривенно, с или без сопутствующей терапии. События произошли у пациентов, получавших премедикацию. Гиперчувствительность, включая анафилаксию, возникала как с предшествующими реакциями гиперчувствительности, так и без них, а также уже при первом введении Актемры [см. Побочные реакции (6.6)]. Актемра для внутривенного применения должна вводиться только медицинским работником с соответствующей медицинской поддержкой для лечения анафилаксии. Для подкожной инъекции Актемры посоветуйте пациентам немедленно обратиться за медицинской помощью, если они испытывают какие-либо симптомы реакции гиперчувствительности. Если возникает анафилаксия или другие реакции гиперчувствительности, немедленно прекратите прием Актемры и навсегда прекратите прием Актемры. Не вводите Актемру пациентам с известной гиперчувствительностью к Актемре [см. Противопоказания (4) и Побочные реакции (6)].
Демиелинизирующие заболевания
Влияние лечения Актемрой на демиелинизирующие расстройства неизвестно, но в клинических исследованиях РА редко сообщалось о рассеянном склерозе и хронической воспалительной демиелинизирующей полинейропатии. Наблюдайте за пациентами на предмет признаков и симптомов, потенциально указывающих на демиелинизирующие расстройства. Лицам, назначающим препарат, следует проявлять осторожность при рассмотрении возможности использования Актемры у пациентов с уже существующими или недавно появившимися демиелинизирующими расстройствами.
Активная болезнь печени и печеночная недостаточность
Лечение Actemra не рекомендуется пациентам с активным заболеванием печени или печеночной недостаточностью [см. Побочные реакции (6.1), Использование в конкретных группах населения (8.6)].
Прививки
Избегайте использования живых вакцин одновременно с Актемрой, поскольку клиническая безопасность не установлена. Нет данных о вторичной передаче инфекции от лиц, получавших живые вакцины, пациентам, получающим Актемру.
Нет данных об эффективности вакцинации пациентов, получающих Актемру. Поскольку ингибирование ИЛ-6 может мешать нормальному иммунному ответу на новые антигены, рекомендуется, чтобы все пациенты, особенно дети или пожилые пациенты, если это возможно, были проинформированы обо всех иммунизациях в соответствии с текущими руководящими принципами иммунизации до начала вакцинации Actemra. терапия.Интервал между вакцинацией живыми вакцинами и началом терапии Актемрой должен соответствовать действующим руководящим принципам вакцинации в отношении иммунодепрессантов.
Побочные реакции
Следующие серьезные побочные реакции описаны в другом месте маркировки:
Поскольку клинические исследования проводятся в самых разных условиях, частота побочных реакций, наблюдаемая в клинических исследованиях одного лекарственного средства, не может быть напрямую сопоставлена с частотой в клинических исследованиях другого препарата и может не предсказывать частоту, наблюдаемую в более широкой популяции пациентов в клинической практике. .
Опыт клинических испытаний пациентов с ревматоидным артритом, леченных внутривенной Актемрой (Актемра-IV)
Данные Actemra-IV при ревматоидном артрите (РА) включают 5 двойных слепых контролируемых многоцентровых исследований. В этих исследованиях пациенты получали монотерапию Актемрой-IV в дозе 8 мг / кг (288 пациентов), Актемрой-IV в дозе 8 мг / кг в комбинации с БПВП (включая метотрексат) (1582 пациента) или Актемрой-IV в дозе 4 мг / кг. комбинация с метотрексатом (774 пациента).
Популяция, подвергшаяся воздействию, включает всех пациентов, участвовавших в регистрационных исследованиях, которые получили хотя бы одну дозу Актемры-IV. Из 4009 пациентов в этой популяции 3577 получали лечение не менее 6 месяцев, 3309 — не менее одного года; Не менее 2 лет прошли лечение 2954 человека, 3 года — 2189 человек.
Все пациенты в этих исследованиях имели активный ревматоидный артрит от умеренной до тяжелой степени. Средний возраст исследуемой популяции составлял 52 года, 82% составляли женщины и 74% составляли европеоид.
Наиболее распространенными серьезными побочными реакциями были серьезные инфекции [см. Предупреждения и меры предосторожности (5.1)]. Наиболее частыми побочными реакциями в контролируемых исследованиях продолжительностью до 24 недель (встречающимися не менее чем у 5% пациентов, получавших монотерапию Актемрой-IV или в комбинации с БПВП), были инфекции верхних дыхательных путей, ринофарингит, головная боль, артериальная гипертензия и повышение уровня АЛТ.
Доля пациентов, которые прекратили лечение из-за каких-либо побочных реакций во время двойных слепых плацебо-контролируемых исследований, составляла 5% для пациентов, принимавших Актемра-IV, и 3% для пациентов, получавших плацебо.Наиболее частыми побочными реакциями, потребовавшими отмены Актемры-IV, были повышенные значения печеночных трансаминаз (согласно требованиям протокола) и серьезные инфекции.
Общие инфекции
За 24 недели контролируемых клинических исследований частота инфекций в группе монотерапии Актемрой-IV составила 119 событий на 100 пациенто-лет и была аналогичной в группе монотерапии метотрексатом. Частота инфекций в группе 4 мг / кг и 8 мг / кг Actemra-IV плюс DMARD составила 133 и 127 событий на 100 пациенто-лет, соответственно, по сравнению со 112 случаями на 100 пациенто-лет в группе плацебо плюс DMARD.Наиболее частыми инфекциями (от 5% до 8% пациентов) были инфекции верхних дыхательных путей и ринофарингит.
Общая частота инфекций, вызванных Actemra-IV, в популяции, подвергшейся воздействию, оставалась совместимой с показателями в контролируемые периоды исследований.
Серьезные инфекции
За 24 недели контролируемых клинических исследований частота серьезных инфекций в группе монотерапии Актемрой-IV составила 3,6 на 100 пациенто-лет по сравнению с 1,5 на 100 пациенто-лет в группе метотрексата.Частота серьезных инфекций в группе 4 мг / кг и 8 мг / кг Actemra-IV плюс DMARD составляла 4,4 и 5,3 события на 100 пациенто-лет, соответственно, по сравнению с 3,9 событий на 100 пациенто-лет в группе плацебо плюс DMARD. .
В популяции, подвергшейся все воздействию, общий уровень серьезных инфекций оставался совместимым с показателями в контролируемые периоды исследований. Наиболее частыми серьезными инфекциями были пневмония, инфекция мочевыводящих путей, целлюлит, опоясывающий лишай, гастроэнтерит, дивертикулит, сепсис и бактериальный артрит.Сообщалось о случаях оппортунистических инфекций [см. Предупреждения и меры предосторожности (5.1)].
В исследовании сердечно-сосудистых исходов WA25204 частота серьезных инфекций в группе Актемры 8 мг / кг внутривенно каждые 4 недели, с или без БПВП, составляла 4,5 на 100 пациенто-лет, а частота серьезных инфекций в группе этанерцепта 50 мг еженедельно подкожно. , с или без БПВП, составляло 3,2 на 100 пациенто-лет. [см. Клинические исследования (14.1)]
Перфорация желудочно-кишечного тракта
В течение 24 недель контролируемых клинических испытаний общая частота перфорации желудочно-кишечного тракта была равна 0.26 событий на 100 пациенто-лет при терапии Актемрой-IV.
В популяции, получавшей все воздействие, общая частота перфорации желудочно-кишечного тракта оставалась совместимой с частотой в контролируемые периоды исследований. Сообщения о перфорации желудочно-кишечного тракта в основном сообщались как осложнения дивертикулита, включая генерализованный гнойный перитонит, перфорацию нижних отделов ЖКТ, свищ и абсцесс. Большинство пациентов, у которых развилась перфорация желудочно-кишечного тракта, одновременно принимали нестероидные противовоспалительные препараты (НПВП), кортикостероиды или метотрексат [см. Предупреждения и меры предосторожности (5.2)]. Относительный вклад этих сопутствующих препаратов по сравнению с Актемрой-IV в развитие перфораций ЖКТ неизвестен.
Инфузионные реакции
За 24 недели контролируемых клинических исследований побочные эффекты, связанные с инфузией (возникающие во время или в течение 24 часов после начала инфузии), были зарегистрированы у 8% и 7% пациентов при приеме 4 мг на кг и 8 мг на кг. Группа Актемра-IV плюс DMARD, соответственно, по сравнению с 5% пациентов в группе плацебо плюс DMARD.Наиболее часто сообщаемым событием при дозе 4 мг на кг и 8 мг на кг во время инфузии была гипертензия (1% для обеих доз), в то время как наиболее часто сообщаемым событием, происходящим в течение 24 часов после окончания инфузии, была головная боль (1% для обе дозы) и кожные реакции (1% для обеих доз), включая сыпь, зуд и крапивницу. Эти события не ограничивали лечение.
Анафилаксия
Реакции гиперчувствительности, требующие прекращения лечения, включая анафилаксию, связанные с Actemra-IV, были зарегистрированы у 0.1% (3 из 2644) в 24-недельных контролируемых испытаниях и 0,2% (8 из 4009) в популяции, подвергшейся все воздействию. Эти реакции обычно наблюдались во время второго-четвертого вливания Актемры-IV. Соответствующее лечение должно быть доступно для немедленного использования в случае серьезной реакции гиперчувствительности [см. Предупреждения и меры предосторожности 5.6)].
Отклонения от нормы
Нейтропения
За 24 недели контролируемых клинических исследований снижение числа нейтрофилов ниже 1000 на мм3 произошло в 1.8% и 3,4% пациентов в группе 4 мг / кг и 8 мг / кг Actemra-IV плюс DMARD, соответственно, по сравнению с 0,1% пациентов в группе плацебо + DMARD. Примерно половина случаев АНК ниже 1000 на мм3 произошла в течение 8 недель после начала терапии. Снижение количества нейтрофилов ниже 500 на мм3 произошло у 0,4% и 0,3% пациентов в группе Актемра-IV плюс БПВП 4 мг на кг и 8 мг на кг соответственно, по сравнению с 0,1% пациентов в группе плацебо плюс БПВП. Не было четкой связи между снижением нейтрофилов ниже 1000 на мм3 и возникновением серьезных инфекций.
В популяции, получавшей все облучение, характер и частота снижения количества нейтрофилов оставались совместимыми с тем, что наблюдалось в контролируемых клинических исследованиях за 24 недели [см. Предупреждения и меры предосторожности (5.4)].
Тромбоцитопения
За 24 недели контролируемых клинических исследований снижение количества тромбоцитов ниже 100000 на мм3 произошло у 1,3% и 1,7% пациентов, получавших 4 мг / кг и 8 мг / кг Actemra-IV в сочетании с DMARD, соответственно, по сравнению с 0,5% пациентов. пациенты, получавшие плацебо и БПВП, без связанных кровотечений.
В популяции, подвергшейся все воздействию, характер и частота снижения количества тромбоцитов оставались совместимыми с тем, что было замечено в контролируемых клинических исследованиях за 24 недели [см. Предупреждения и меры предосторожности 5.4)].
Повышенные ферменты печени
Нарушения ферментов печени суммированы в таблице 1. У пациентов, у которых наблюдается повышение уровня ферментов печени, изменение схемы лечения, такое как уменьшение дозы сопутствующего БПВП, прерывание приема Актемры-IV или снижение дозы Актемры-IV, приводило к снижению или нормализация ферментов печени [см. Администрация и дозировка (2.6)]. Это повышение не было связано с клинически значимым повышением уровня прямого билирубина и не было связано с клиническими признаками гепатита или печеночной недостаточности [см. Предупреждения и меры предосторожности (5.3, 5.4)].
| Актемра 8 мг на кг МОНОТЕРАПИЯ | Метотрексат | Актемра 4 мг на кг + БПВП | Актемра 8 мг на кг + БПВП | Плацебо + БПВП | |
|---|---|---|---|---|---|
| N = 288 (%) | N = 284 (%) | N = 774 (%) | N = 1582 (%) | N = 1170 (%) | |
| ULN = Верхний предел нормы | |||||
| AST (Е / л) | |||||
| > ULN до 3 × ULN | 22 | 26 | 34 | 41 | 17 |
| > 3 × ULN до 5 × ULN | 0.3 | 2 | 1 | 2 | 0,3 |
| > 5 × ULN | 0,7 | 0,4 | 0,1 | 0,2 | <0,1 |
| ALT (Ед / л) | |||||
| > ULN до 3 × ULN | 36 | 33 | 45 | 48 | 23 |
| > 3 × ULN до 5 × ULN | 1 | 4 | 5 | 5 | 1 |
| > 5 × ULN | 0.7 | 1 | 1,3 | 1,5 | 0,3 |
В популяции, получавшей все воздействие, повышение уровня АЛТ и АСТ оставалось совместимым с тем, что наблюдалось в 24-недельных контролируемых клинических испытаниях.
В исследовании WA25204 из 1538 пациентов с РА средней и тяжелой степени (см. Раздел 14, Клинические исследования), получавших тоцилизумаб, повышение АЛТ или АСТ> 3 × ВГН произошло у 5,3% и 2,2% пациентов соответственно. Сообщалось об одном серьезном случае лекарственного гепатита с гипербилирубинемией в связи с тоцилизумабом.
Липиды
Повышение липидных параметров (общий холестерин, ЛПНП, ЛПВП, триглицериды) впервые было оценено через 6 недель после начала применения Актемры-IV в контролируемых 24-недельных клинических испытаниях. В этот момент наблюдался рост, который после этого оставался стабильным. Повышение уровня триглицеридов до уровней выше 500 мг / дл наблюдалось редко. Изменения других липидных параметров по сравнению с исходным уровнем до 24-й недели были оценены и суммированы ниже:
- —
- Среднее значение ЛПНП увеличилось на 13 мг на дл в группе Actemra 4 мг на кг + DMARD, 20 мг на дл в группе Actemra 8 мг на кг + DMARD и на 25 мг на дл в группе монотерапии Actemra 8 мг на кг.
- –
- Среднее значение ЛПВП увеличилось на 3 мг на дл в группе Actemra 4 мг на кг + DMARD, 5 мг на дл в группе Actemra 8 мг на кг + DMARD и на 4 мг на дл в группе монотерапии Actemra 8 мг на кг.
- –
- Среднее соотношение LDL / HDL увеличилось в среднем на 0,14 в группе Actemra 4 мг на кг + DMARD, на 0,15 в группе Actemra 8 мг на кг + DMARD и на 0,26 в группе монотерапии Actemra 8 мг на кг.
- – Отношения
- ApoB / ApoA1 практически не изменились у пациентов, получавших Actemra.
Повышенные липиды реагировали на гиполипидемические агенты.
В популяции, получавшей все воздействие, повышение липидных параметров оставалось таким же, как и в 24-недельных контролируемых клинических испытаниях.
Иммуногенность
Как и все терапевтические белки, существует потенциал иммуногенности. Обнаружение образования антител во многом зависит от чувствительности и специфичности анализа. Кроме того, наблюдаемая частота положительности антител (включая нейтрализующие антитела) в анализе может зависеть от нескольких факторов, включая методологию анализа, обработку образцов, время сбора образцов, сопутствующие лекарства и основное заболевание.По этим причинам сравнение встречаемости антител к тоцилизумабу в исследованиях, описанных ниже, с частотой встречаемости антител в других исследованиях или к другим препаратам может вводить в заблуждение.
За 24 недели контролируемых клинических исследований в общей сложности 2876 пациентов были протестированы на антитела к тоцилизумабу. У сорока шести пациентов (2%) развились положительные антитела к тоцилизумабу, из которых у 5 была ассоциированная, значимая с медицинской точки зрения реакция гиперчувствительности, приводящая к отмене.У 30 пациентов (1%) выработались нейтрализующие антитела.
Злокачественные новообразования
В течение 24 недель контролируемого периода исследований у пациентов, получавших Актемру-IV, было диагностировано 15 злокачественных новообразований, по сравнению с 8 злокачественными новообразованиями у пациентов в контрольных группах. Частота с поправкой на экспозицию была сходной в группах Actemra-IV (1,32 случая на 100 пациенто-лет) и в группе плацебо плюс DMARD (1,37 случая на 100 пациенто-лет).
В популяции, получавшей все облучение, частота злокачественных новообразований оставалась совместимой с частотой, наблюдаемой в течение 24 недель контролируемого периода [см. Предупреждения и меры предосторожности (5.5)].
Другие побочные реакции
Побочные реакции, возникающие у 2% или более пациентов при приеме 4 или 8 мг / кг препарата Актемра-IV плюс DMARD и по крайней мере на 1% более выраженные, чем наблюдаемые у пациентов, получавших плацебо и DMARD, суммированы в таблице 2.
| 24-недельная фаза 3 Контролируемое исследование населения | |||||
|---|---|---|---|---|---|
| Актемра 8 мг на кг МОНОТЕРАПИЯ | Метотрексат | Актемра 4 мг на кг + БПВП | Актемра 8 мг на кг + БПВП | Плацебо + БПВП | |
| Предпочтительный срок | N = 288 (%) | N = 284 (%) | N = 774 (%) | N = 1582 (%) | N = 1170 (%) |
| Инфекция верхних дыхательных путей | 7 | 5 | 6 | 8 | 6 |
| Ринофарингит | 7 | 6 | 4 | 6 | 4 |
| Головная боль | 7 | 2 | 6 | 5 | 3 |
| Гипертония | 6 | 2 | 4 | 4 | 3 |
| ALT увеличен | 6 | 4 | 3 | 3 | 1 |
| Головокружение | 3 | 1 | 2 | 3 | 2 |
| Бронхит | 3 | 2 | 4 | 3 | 3 |
| Сыпь | 2 | 1 | 4 | 3 | 1 |
| Изъязвление рта | 2 | 2 | 1 | 2 | 1 |
| Боль в животе вверху | 2 | 2 | 3 | 3 | 2 |
| Гастрит | 1 | 2 | 1 | 2 | 1 |
| Повышенная трансаминаза | 1 | 5 | 2 | 2 | 1 |
Среди других нечастых и значимых с медицинской точки зрения побочных реакций, встречающихся с частотой менее 2% у пациентов с ревматоидным артритом, получавших Актемру-IV в контролируемых исследованиях, были:
Инфекции и инвазии: простой герпес полости рта
Заболевания желудочно-кишечного тракта: стоматит, язва желудка
Исследования: вес увеличился, билирубин общий
Нарушения со стороны крови и лимфатической системы: лейкопения
Общие нарушения и состояния в месте введения: периферический отек
Нарушения со стороны органов дыхания, грудной клетки и средостения: одышка, кашель
Заболевания глаз: конъюнктивит
Нарушения со стороны почек: нефролитиаз
Эндокринные расстройства: гипотиреоз
Опыт клинических испытаний пациентов с ревматоидным артритом, получавших подкожную Actemra (Actemra-SC)
Данные Actemra-SC при ревматоидном артрите (РА) включают 2 двойных слепых контролируемых многоцентровых исследования.Исследование SC-I было исследованием не меньшей эффективности, в котором сравнивалась эффективность и безопасность тоцилизумаба в дозе 162 мг, вводимого каждую неделю подкожно и 8 мг / кг внутривенно каждые четыре недели, у 1262 взрослых пациентов с ревматоидным артритом. Исследование SC-II было плацебо-контролируемым исследованием превосходства, в котором оценивалась безопасность и эффективность тоцилизумаба в дозе 162 мг, вводимого через неделю подкожно или плацебо, у 656 пациентов. Все пациенты в обоих исследованиях получали базовые небиологические БПВП.
Безопасность, наблюдаемая для Actemra-SC, вводимого подкожно, соответствовала известному профилю безопасности внутривенного введения Actemra, за исключением реакций в месте инъекции (ISR), которые были более частыми для Actemra-SC, чем при подкожных инъекциях плацебо (IV группа).
Реакции в месте инъекции
За 6-месячный контрольный период в группе SC-I частота ISR составляла 10,1% (64/631) и 2,4% (15/631) для еженедельных групп Actemra-SC и плацебо SC (IV-группа), соответственно. В SC-II частота ISR составляла 7,1% (31/437) и 4,1% (9/218) через каждую вторую неделю в группах Actemra-SC и плацебо, соответственно. Эти ISR (включая эритему, зуд, боль и гематому) были от легкой до умеренной по степени тяжести. Большинство из них исчезли без какого-либо лечения, и ни один из них не потребовал отмены препарата.
Иммуногенность
За 6-месячный контрольный период в группе SC-I у 0,8% (5/625) в группе Actemra-SC и у 0,8% (5/627) в группе внутривенного введения выработались антитела против тоцилизумаба; из них все выработали нейтрализующие антитела. В группе SC-II 1,6% (7/434) в группе Actemra-SC по сравнению с 1,4% (3/217) в группе плацебо вырабатывали антитела против тоцилизумаба; из них 1,4% (6/434) в группе Actemra-SC и 0,5% (1/217) в группе плацебо также выработали нейтрализующие антитела.
В общей сложности 1454 (> 99%) пациентов, получавших Актемра-СК во всей группе воздействия, были протестированы на антитела к тоцилизумабу.У 13 пациентов (0,9%) развились антитела против тоцилизумаба, из них у 12 пациентов (0,8%) развились нейтрализующие антитела.
Скорость соответствует предыдущему опыту внутривенного введения. Корреляции развития антител с побочными эффектами или потерей клинического ответа не наблюдалось.
Отклонения от нормы
Нейтропения
Во время рутинного лабораторного мониторинга в ходе 6-месячных контролируемых клинических исследований снижение количества нейтрофилов ниже 1 × 109 / л произошло у 2.9% и 3,7% пациентов получали Актемра-СК еженедельно и раз в две недели соответственно.
Не было четкой связи между снижением нейтрофилов ниже 1 × 109 / л и возникновением серьезных инфекций.
Тромбоцитопения
В ходе рутинного лабораторного мониторинга в 6-месячных контролируемых клинических испытаниях Actemra-SC ни у одного из пациентов не было снижения количества тромбоцитов до ≤50 000 / мм3.
Повышенные ферменты печени
Во время рутинного лабораторного мониторинга в ходе 6-месячных контролируемых клинических испытаний повышение АЛТ или АСТ ≥3 × ВГН произошло у 6.5% и 1,4% пациентов получали Актемра-СК еженедельно и 3,4% и 0,7% пациентов получали Актемра-СК раз в две недели.
Повышение липидных параметров
Во время рутинного лабораторного мониторинга в 6-месячных клинических испытаниях Actemra-SC, 19% пациентов получали дозу еженедельно, 19,6% пациентов получали дозу раз в две недели, а у 10,2% пациентов, получавших плацебо, наблюдалось стойкое повышение общего холестерина> 6,2 ммоль / л ( 240 мг / дл), при этом у 9%, 10,4% и 5,1% наблюдается устойчивое повышение ЛПНП до 4.1 ммоль / л (160 мг / дл) приема Актемра-СК еженедельно, раз в две недели и плацебо, соответственно.
Опыт клинических испытаний у пациентов с гигантоклеточным артериитом, получавших подкожную Actemra (Actemra-SC)
Безопасность подкожного введения Актемры (тоцилизумаба) изучалась в одном исследовании фазы III (WA28119) с участием 251 пациента с ГКА. Общая продолжительность пациенто-лет в группе Actemra GCA, получавшей все экспозиции, составила 138,5 пациенто-лет в течение 12-месячной двойной слепой плацебо-контролируемой фазы исследования.Общий профиль безопасности, наблюдаемый в группах лечения Актемрой, в целом соответствовал известному профилю безопасности Актемры. В целом частота инфекций у пациентов с ГКА была выше, чем у пациентов с РА. Частота инфекций / серьезных инфекционных событий составляла 200,2 / 9,7 событий на 100 пациенто-лет в группе еженедельной терапии Актемра и 160,2 / 4,4 событий на 100 пациенто-лет в группе Актемры каждые две недели по сравнению с 156,0 / 4,2 события на 100 пациенто-лет в группе. плацебо + прием преднизона на 26 неделе и 210.2 / 12,5 событий на 100 пациенто-лет в группах плацебо + 52 недели постепенного снижения.
Опыт клинических исследований у пациентов с полиартикулярным ювенильным идиопатическим артритом, получавших внутривенное введение Actemra (Actemra-IV)
Безопасность Актемры-IV изучалась на 188 педиатрических пациентах в возрасте от 2 до 17 лет с ПЮИА, у которых был неадекватный клинический ответ или была непереносимость метотрексата. Общее облучение пациентов в популяции, получавшей все облучение Actemra-IV (определяемой как пациенты, получившие хотя бы одну дозу Actemra-IV), составило 184 человека.4 пациенто-года. Исходно примерно половина пациентов принимала пероральные кортикостероиды и почти 80% принимали метотрексат. В целом типы побочных реакций на лекарства у пациентов с ПЮИА соответствовали тем, которые наблюдались у пациентов с РА и сЮИА [см. Побочные реакции (6.1 и 6.6)].
Инфекции
Частота инфекций в популяции, подвергшейся воздействию Actemra-IV, составила 163,7 на 100 пациенто-лет. Наиболее частыми наблюдаемыми явлениями были ринофарингит и инфекции верхних дыхательных путей.Частота серьезных инфекций была численно выше у пациентов с массой тела менее 30 кг, получавших тоцилизумаб в дозе 10 мг / кг (12,2 на 100 пациенто-лет), по сравнению с пациентами с массой тела 30 кг и более, получавших тоцилизумаб в дозе 8 мг / кг (4,0 на 100 пациентов). пациенто-лет). Частота инфекций, приводящих к прерыванию приема препарата, также была численно выше у пациентов с массой тела менее 30 кг, получавших тоцилизумаб в дозе 10 мг / кг (21%), по сравнению с пациентами с массой тела 30 кг и более, получавших тоцилизумаб в дозе 8 мг / кг (8%). ).
Инфузионные реакции
У пациентов с ПЮИА реакции, связанные с инфузией, определяются как все события, происходящие во время или в течение 24 часов после инфузии. В популяции, получавшей все воздействие Actemra-IV, у 11 пациентов (6%) произошло событие во время инфузии, а у 38 пациентов (20,2%) произошло событие в течение 24 часов после инфузии. Наиболее частыми явлениями, возникающими во время инфузии, были головная боль, тошнота и гипотензия, а в течение 24 часов после инфузии — головокружение и гипотензия.В целом, побочные реакции на лекарства, наблюдаемые во время или в течение 24 часов после инфузии, были аналогичны по своей природе тем, которые наблюдались у пациентов с РА и сЮИА [см. Побочные реакции (6.1 и 6.6)].
Не поступало сообщений о клинически значимых реакциях гиперчувствительности, связанных с тоцилизумабом и требующих прекращения лечения.
Иммуногенность
У одного пациента в группе 10 мг / кг менее 30 кг развились положительные антитела против тоцилизумаба без развития реакции гиперчувствительности, и впоследствии он выбыл из исследования.
Отклонения от нормы
Нейтропения
Во время рутинного лабораторного мониторинга в популяции, подвергшейся воздействию Actemra-IV, снижение количества нейтрофилов ниже 1 × 109 на литр произошло у 3,7% пациентов.
Не было четкой связи между снижением нейтрофилов ниже 1 × 109 на л и возникновением серьезных инфекций.
Тромбоцитопения
Во время рутинного лабораторного мониторинга в популяции, получавшей Actemra-IV, у 1% пациентов наблюдалось снижение количества тромбоцитов на уровне или менее 50 000 на мм3 без связанных кровотечений.
Повышенные ферменты печени
Во время рутинного лабораторного мониторинга в группе Actemra-IV во всей популяции, подвергшейся воздействию, повышение уровня АЛТ или АСТ на уровне или более чем в 3 раза выше ULN произошло у 4% и менее 1% пациентов, соответственно.
Липиды
Во время рутинного лабораторного мониторинга в популяции, получавшей тоцилизумаб, во всей популяции, подверженной воздействию тоцилизумаба, повышение общего холестерина более чем на 1,5-2 × ВГН произошло у одного пациента (0,5%), а повышение уровня ЛПНП более чем на 1,5-2 × ВГН произошло у одного пациента (0.5%).
Опыт клинических исследований у пациентов с полиартикулярным ювенильным идиопатическим артритом, получавших подкожную Actemra (Actemra-SC)
Безопасность Actemra-SC изучалась на 52 педиатрических пациентах в возрасте от 1 до 17 лет с PJIA, у которых был неадекватный клинический ответ или была непереносимость метотрексата. Общее воздействие на пациентов в популяции PJIA Actemra-SC (определяемой как пациенты, получившие по крайней мере одну дозу Actemra-SC и с учетом прекращения лечения) составило 49.5 пациенто-лет. В целом безопасность, наблюдаемая для Актемры, вводимой подкожно, соответствовала известному профилю безопасности Актемры внутривенно, за исключением реакций в месте инъекции (ISR) и нейтропении.
Реакции в месте инъекции
В течение 1-летнего исследования частота ISR составила 28,8% (15/52) у пациентов, получавших PJIA, получавших Actemra-SC. Эти ISR наблюдались у большей части пациентов с массой тела 30 кг и выше (44,0%) по сравнению с пациентами с массой тела менее 30 кг (14.8%). Все ISR были легкой степени тяжести, и ни один из ISR не требовал прекращения лечения или прерывания дозы. Более высокая частота ISR наблюдалась у пациентов с PJIA, получавших Actemra-SC, по сравнению с тем, что наблюдалось у взрослых пациентов с RA или GCA [см. Побочные реакции (6.1 и 6.3)].
Иммуногенность
У трех пациентов, 1 пациента с массой тела менее 30 кг и 2 пациентов с массой тела 30 кг или выше, развились положительные антитела против тоцилизумаба с нейтрализующим потенциалом без развития серьезной или клинически значимой реакции гиперчувствительности.Один пациент впоследствии выбыл из исследования.
Нейтропения
Во время рутинного лабораторного мониторинга в популяции, получавшей Actemra-SC, у всех облученных пациентов снижение количества нейтрофилов ниже 1 × 109 на литр произошло у 15,4% пациентов и чаще наблюдалось у пациентов с массой тела менее 30 кг (25,9%) по сравнению с пациенты с массой тела 30 кг и выше (4,0%). Не было четкой связи между снижением нейтрофилов ниже 1 × 109 на литр и возникновением серьезных инфекций.
Опыт клинических испытаний у пациентов с системным ювенильным идиопатическим артритом, получавших внутривенное введение Актемры (Актемра-IV)
Данные, описанные ниже, отражают воздействие Актемры-IV в одном рандомизированном двойном слепом плацебо-контролируемом исследовании 112 педиатрических пациентов с сЮИА в возрасте от 2 до 17 лет, у которых был неадекватный клинический ответ на нестероидные противовоспалительные препараты (НПВП). или кортикостероиды из-за токсичности или отсутствия эффективности. Исходно примерно половина пациентов принимала 0.Кортикостероиды 3 мг / кг / день или более, и почти 70% принимали метотрексат. Испытание включало 12-недельную контролируемую фазу, за которой следовало открытое продление. В течение 12 недель двойного слепого контролируемого клинического исследования 75 пациентов получали лечение Актемрой-IV (8 или 12 мг на кг в зависимости от массы тела). Через 12 недель или во время побега из-за обострения болезни пациенты получали Актемру-IV в открытой расширенной фазе.
Наиболее частыми нежелательными явлениями (не менее 5%), наблюдаемыми у пациентов, получавших Актемру-IV, в течение 12-недельной контролируемой части исследования, были: инфекция верхних дыхательных путей, головная боль, ринофарингит и диарея.
Инфекции
В 12-недельной контролируемой фазе частота всех инфекций в группе Actemra-IV составляла 345 на 100 пациенто-лет и 287 на 100 пациенто-лет в группе плацебо. В открытом расширении в течение средней продолжительности лечения 73 недели общая частота инфекций составила 304 на 100 пациенто-лет.
В 12-недельной контролируемой фазе частота серьезных инфекций в группе Actemra-IV составила 11,5 на 100 пациенто-лет. В открытом расширении продолжительности лечения в течение 73 недель общее количество серьезных инфекций составило 11.4 на 100 пациенто-лет. Наиболее часто регистрируемые серьезные инфекции включали пневмонию, гастроэнтерит, ветряную оспу и средний отит.
Синдром активации макрофагов
В 12-недельном контролируемом исследовании ни у одного пациента ни в одной группе лечения не наблюдался синдром активации макрофагов (MAS) во время назначенного лечения; У 3 из 112 (3%) развилась МАС во время открытого лечения препаратом Актемра-IV. Один пациент в группе плацебо избежал приема Актемры-IV в дозе 12 мг / кг на 2-й неделе из-за тяжелой активности заболевания и, в конечном итоге, развил MAS на 70-й день.У двух дополнительных пациентов развился МАС в течение длительного периода. Всем 3 пациентам доза Актемры-IV была прервана (2 пациента) или отменена (1 пациент) из-за события MAS, получено лечение, и MAS разрешился без последствий. Основываясь на ограниченном числе случаев, частота MAS не кажется повышенной в опыте клинической разработки Actemra-IV SJIA; однако окончательных выводов сделать нельзя.
Инфузионные реакции
Пациенты не получали премедикации, однако большинство пациентов получали сопутствующие кортикостероиды в рамках фонового лечения сЮИА.Реакции, связанные с инфузией, определялись как все события, происходящие в течение или в течение 24 часов после инфузии. В 12-недельной контролируемой фазе у 4% пациентов, получавших Актемра-IV и 0% пациентов, получавших плацебо, наблюдались события, происходящие во время инфузии. Одно событие (ангионевротический отек) было сочтено серьезным и опасным для жизни, и пациент был исключен из исследуемого лечения.
В течение 24 часов после инфузии у 16% пациентов в группе лечения Actemra-IV и у 5% пациентов в группе плацебо произошло событие.В группе Actemra-IV явления включали сыпь, крапивницу, диарею, дискомфорт в эпигастрии, артралгию и головную боль. Одно из этих событий, крапивница, было признано серьезным.
Анафилаксия
Анафилаксия была зарегистрирована у 1 из 112 пациентов (менее 1%), получавших Actemra-IV во время контролируемого и открытого расширенного исследования [см. Предупреждения и меры предосторожности (5.6)].
Иммуногенность
Все 112 пациентов были проверены на антитела к тоцилизумабу на исходном уровне.У двух пациентов развились положительные антитела против тоцилизумаба: у одного из этих пациентов возникли серьезные побочные эффекты в виде крапивницы и ангионевротического отека, соответствующие анафилактической реакции, которая привела к отмене; у другого пациента развился синдром активации макрофагов во время терапии ухода, и он был исключен из исследования.
Отклонения от нормы
Нейтропения
Во время рутинного мониторинга в 12-недельной контролируемой фазе снижение нейтрофилов ниже 1 × 109 на литр произошло у 7% пациентов в группе Actemra-IV и ни у одного пациента в группе плацебо.В открытом расширении в течение средней продолжительности лечения 73 недели снижение количества нейтрофилов произошло у 17% пациентов из группы Actemra-IV. Не было четкой связи между снижением нейтрофилов ниже 1 × 109 на литр и возникновением серьезных инфекций.
Тромбоцитопения
Во время рутинного наблюдения в 12-недельной контролируемой фазе у 1% пациентов в группе Актемры-IV и у 3% в группе плацебо наблюдалось снижение количества тромбоцитов не более чем до 100 000 на мм3.
В открытом расширении в течение средней продолжительности лечения 73 недели снижение количества тромбоцитов произошло у 4% пациентов в группе Actemra-IV без связанного кровотечения.
Повышенные ферменты печени
Во время рутинного лабораторного мониторинга в 12-недельной контролируемой фазе повышение уровня АЛТ или АСТ на уровне 3 × ULN или выше произошло у 5% и 3% пациентов, соответственно, в группе Актемры-IV и у 0% пациентов, получавших плацебо.
В открытом расширении в течение средней продолжительности лечения 73 недели повышение уровня АЛТ или АСТ на уровне 3 × ВГН или выше произошло у 13% и 5% пациентов, получавших Актемра-IV, соответственно.
Липиды
Во время рутинного лабораторного мониторинга в течение 12-недельной контролируемой фазы повышение общего холестерина более чем на 1,5 × ULN — 2 × ULN произошло у 1,5% группы Actemra-IV и у 0% пациентов, получавших плацебо. Повышение уровня ЛПНП более 1,5 × ВГН — 2 × ВГН произошло у 1,9% пациентов в группе Актемры-IV и 0% в группе плацебо.
В открытом расширенном исследовании в течение средней продолжительности лечения 73 недели, картина и частота повышения липидных параметров оставались совместимыми с данными 12-недельного контролируемого исследования.
Опыт клинических испытаний у пациентов с системным ювенильным идиопатическим артритом, получавших подкожную Actemra (Actemra-SC)
Профиль безопасности Actemra-SC был изучен на 51 педиатрическом пациенте в возрасте от 1 до 17 лет с сЮИА, у которого был неадекватный клинический ответ на НПВП и кортикостероиды. В целом безопасность, наблюдаемая при подкожном введении Actemra, соответствовала известному профилю безопасности внутривенного введения Actemra, за исключением ISR, где более высокая частота наблюдалась у пациентов с SJIA, получавших Actemra-SC, по сравнению с пациентами с PJIA и взрослыми пациентами с RA или GCA [ см. Побочные реакции (6.2 и 6.3)].
Реакции в месте инъекции (ISR)
В общей сложности 41,2% (21/51) пациентов с сЮИА испытали ISR на Actemra-SC. Наиболее частыми ISR были эритема, зуд, боль и припухлость в месте инъекции. Большинство сообщенных ISR были событиями степени 1, и все зарегистрированные ISR были несерьезными, и ни один из них не требовал прекращения лечения или прерывания дозы.
Иммуногенность
Сорок шесть из 51 (90,2%) пациента, которые были протестированы на антитела против тоцилизумаба на исходном уровне, имели по крайней мере один результат скринингового анализа после исходного уровня.После исходного уровня ни у одного пациента не развились положительные антитела к тоцилизумабу.
Опыт клинических испытаний у пациентов с синдромом высвобождения цитокинов, получавших лечение внутривенным введением Актемры (Актемра-IV)
В ретроспективном анализе объединенных данных по результатам нескольких клинических испытаний 45 пациентов получали тоцилизумаб 8 мг / кг (12 мг / кг для пациентов с массой тела менее 30 кг) с дополнительными высокими дозами кортикостероидов или без них при тяжелой или опасной для жизни CAR CRS, индуцированный Т-клетками. В среднем вводили 1 дозу тоцилизумаба (диапазон 1–4 дозы).Не сообщалось о побочных реакциях, связанных с тоцилизумабом [см. Клинические исследования (14.7)].
Опыт постмаркетинга
Следующие побочные реакции были выявлены во время использования Actemra после утверждения. Поскольку об этих реакциях сообщается добровольно из популяции неопределенного размера, не всегда возможно надежно оценить их частоту или установить причинную связь с воздействием наркотиков.
Лекарственные взаимодействия
Сопутствующие препараты для лечения взрослых по показаниям
У пациентов с РА популяционные фармакокинетические анализы не выявили какого-либо влияния метотрексата (МТ), нестероидных противовоспалительных препаратов или кортикостероидов на клиренс тоцилизумаба.Одновременное введение однократной внутривенной дозы 10 мг / кг Актемры с 10-25 мг метотрексата один раз в неделю не оказало клинически значимого влияния на экспозицию метотрексата. Actemra не изучалась в сочетании с биологическими DMARD, такими как антагонисты TNF [см. Администрация и дозировка (2.1)].
У пациентов с ГКА не наблюдалось никакого влияния сопутствующего кортикостероида на воздействие тоцилизумаба.
Взаимодействие с субстратами CYP450
Цитохром P450 в печени подавляется инфекционными и воспалительными стимулами, включая цитокины, такие как IL-6.Подавление передачи сигналов IL-6 у пациентов с РА, получавших тоцилизумаб, может восстанавливать активность CYP450 до более высоких уровней, чем в отсутствие тоцилизумаба, что приводит к усилению метаболизма препаратов, которые являются субстратами CYP450. Исследования in vitro показали, что тоцилизумаб может влиять на экспрессию нескольких ферментов CYP, включая CYP1A2, CYP2B6, CYP2C9, CYP2C19, CYP2D6 и CYP3A4. Его влияние на CYP2C8 или переносчики неизвестно. Исследования in vivo с омепразолом, метаболизируемым CYP2C19 и CYP3A4, и симвастатином, метаболизируемым CYP3A4, показали снижение воздействия на 28% и 57% через неделю после однократного приема Актемры, соответственно.Влияние тоцилизумаба на ферменты CYP может быть клинически значимым для субстратов CYP450 с узким терапевтическим индексом, когда доза подбирается индивидуально. После начала или прекращения приема Актемры у пациентов, получающих лечение этими типами лекарственных средств, следует проводить терапевтический мониторинг эффекта (например, варфарина) или концентрации лекарства (например, циклоспорина или теофиллина), а также индивидуальную дозу лекарственного средства, скорректированную по мере необходимости. Соблюдайте осторожность при одновременном назначении Актемры с субстратами CYP3A4, когда снижение эффективности нежелательно, например.g., оральные контрацептивы, ловастатин, аторвастатин и т. д. Влияние тоцилизумаба на активность фермента CYP450 может сохраняться в течение нескольких недель после прекращения терапии [см. Клиническая фармакология (12.3)].
Живые вакцины
Избегайте использования живых вакцин одновременно с Actemra [см. Предупреждения и меры предосторожности (5.9)].
ИСПОЛЬЗОВАНИЕ В КОНКРЕТНЫХ НАСЕЛЕНИЯХ
Беременность
Регистр беременных
Существует регистр беременных, в котором отслеживаются исходы беременности у женщин, подвергшихся воздействию Актемры во время беременности.Врачам рекомендуется регистрировать пациентов, а беременным женщинам рекомендуется регистрироваться по телефону 1-877-311-8972.
Обзор рисков
Ограниченных доступных данных о применении Актемры у беременных женщин недостаточно, чтобы определить, существует ли связанный с приемом препарата риск серьезных врожденных дефектов и выкидыша. Моноклональные антитела, такие как тоцилизумаб, активно переносятся через плаценту в течение третьего триместра беременности и могут повлиять на иммунный ответ у новорожденного, подвергшегося воздействию внутриутробного периода [см. Клинические соображения].В исследованиях репродукции животных внутривенное введение тоцилизумаба обезьянам Cynomolgus во время органогенеза приводило к аборту / гибели эмбриона и плода в дозах в 1,25 раза и выше, чем максимальная рекомендуемая доза для человека при внутривенном введении 8 мг на кг каждые 2-4 недели. Литература на животных предполагает, что ингибирование передачи сигналов IL-6 может мешать созреванию и дилатации шейки матки и сократительной активности миометрия, что приводит к потенциальной задержке родов [см. Данные]. Исходя из данных о животных, существует потенциальный риск для плода.
Предполагаемый фоновый риск серьезных врожденных дефектов и выкидыша для указанной группы населения неизвестен. Все беременности имеют фоновый риск врожденного порока, потери или других неблагоприятных исходов. В общей популяции США оценочный фоновый риск серьезных врожденных дефектов и выкидыша при клинически признанных беременностях составляет от 2 до 4% и от 15 до 20%, соответственно.
Клинические аспекты
Побочные реакции у плода / новорожденного
Моноклональные антитела все чаще переносятся через плаценту по мере прогрессирования беременности, причем наибольшее их количество переносится в третьем триместре.Перед введением живых или живых аттенуированных вакцин младенцам, подвергшимся воздействию Actemra in utero, следует учитывать риски и преимущества [см. Предупреждения и меры предосторожности 5.9)]
Данные
Данные о животных
Было проведено исследование токсичности развития эмбриона и плода, в котором беременных обезьян Cynomolgus вводили внутривенно тоцилизумаб в суточных дозах 2, 10 или 50 мг / кг во время органогенеза с 20-50 дня беременности (GD). Хотя не было доказательств тератогенного / дисморфогенного эффекта при любой дозе, тоцилизумаб приводил к увеличению частоты абортов / гибели эмбриона и плода при дозах 1.В 25 и более раз MRHD при внутривенном введении при внутривенных дозах для матери 10 и 50 мг / кг. Тестирование мышиного аналога тоцилизумаба на мышах не дало никаких доказательств вреда для потомства во время пре- и постнатальной фазы развития при внутривенной дозе 50 мг / кг с лечением каждые три дня от имплантации (GD 6) до послеродового дня. 21 (отлучение от груди). Не было доказательств каких-либо функциональных нарушений развития и поведения, способности к обучению, иммунной компетентности и фертильности потомства.
Роды связаны со значительным увеличением IL-6 в шейке матки и миометрии. Литература предполагает, что ингибирование передачи сигналов IL-6 может мешать созреванию и дилатации шейки матки, а также сократительной активности миометрия, что приводит к потенциальной задержке родов. У мышей с дефицитом IL-6 (116 — / — нулевые мыши) роды были отложены по сравнению с мышами дикого типа (116 + / +). Введение рекомбинантного IL-6 мышам с нулевым статусом 116 — / — восстановило нормальное время доставки.
Лактация
Обзор рисков
Нет информации о присутствии тоцилизумаба в грудном молоке, воздействии препарата на грудного ребенка или влиянии препарата на выработку молока.Материнский иммуноглобулин G (IgG) присутствует в материнском молоке. Если тоцилизумаб попадает в грудное молоко, эффекты местного воздействия на желудочно-кишечный тракт и потенциальное ограниченное системное воздействие тоцилизумаба на младенца неизвестны. Отсутствие клинических данных во время кормления грудью не позволяет точно определить риск Actemra для младенца во время кормления грудью; следовательно, преимущества для развития и здоровья o
Рынок репо «сломан», и вливания ФРС не являются долгосрочным решением, предупреждают рыночные профи
- Последний
- Выборы 2020
- Список наблюдения
- Рынки
- Инвестиции
- Barron’s
- Личные финансы
- Экономика
- Выход на пенсию
- Коронавирус
- Видеоцентр
- Комментарий
- Больше Самый последний Выборы 2020 Список наблюдения Рынки Инвестирование Barron’s Личные финансы Экономика Выход на пенсию Коронавирус Видео Центр Комментарий
- Настройки учетной записи
- Войти
- Зарегистрироваться
- Дом
- Последние новости
- Список наблюдения
- Рынки
- U.S. Markets
- Канада
- Европа и Ближний Восток
- Азия
- Развивающиеся рынки
- Латинская Америка
- Рыночные данные
- Инвестирование
- Barron’s
- Лучшие новые идеи
- Акции
- IPO
- Паевые инвестиционные фонды
- ETFs
- Параметры
- Облигации
- Товары
- Валюты
- Криптовалюты
- Фьючерсы
- Центр финансовых консультантов
- Каннабис
Актовегин при гипертонии
Содержание
- 1 Состав и форма выпуска
- 2 Как это работает?
- 3 Безопасность препарата
- 4 Показания
- 5 Инструкция по применению «Актовегина» под давлением
- 6 Противопоказания и побочные эффекты
- 7 Продажа, хранение и срок годности
- 8 Аналогичные препараты
Как действует Актовегин применять при гипертонии, понижает или повышает артериальное давление? Этот препарат, основное назначение которого — расширение кровеносных сосудов, оказывает прямое влияние на артериальное давление, снижая его высокие показатели.Фармацевтический препарат обладает слабо выраженным гипотензивным действием, поэтому его обычно назначают при не очень высоком давлении или в сочетании с другими подобными лекарствами, направленными на уравновешивание артериального давления.
Состав и форма выпуска
Препарат «Актовегин» продается в нескольких формах, каждая из которых имеет в качестве действующего вещества гемодериват из крови телят и различные вспомогательные компоненты:
| Лекарственная форма | Состав |
| Таблетки | Пищевой эмульгатор E572, повидон, целлюлоза, тальк, гуммиарабик, озокерит, фталат гидроксипропилметилцеллюлозы, фиксатор запаха, микрогель 6000, пищевой краситель E171, сахароза |
| Мазь | |
| Мазь липосервика | Вазелин, цетилпеппер дистиллированная вода |
| Гель | Целлюлозная камедь, пищевая добавка E1520, очищенная вода, кальциевая соль молочной кислоты, консервант E218, пропилпарабен |
| Инфузионный раствор | Очищенная вода, хлорид натрия |
| Концентрат актовегина, д / и воды, натриевая соль соляной кислоты |
Как это работает?
Препарат «Актовегин» улучшает кислородный и энергетический обмен в тканях.Лекарственный препарат «Актовегин» усиливает процессы метаболизма кислорода и глюкозы в тканях, эффективен при лечении нарушений мозгового кровообращения с поражением тканей мозга, невоспалительных заболеваний головного мозга. Актовегин не может повышать давление, а наоборот, снижает его. Именно такое действие препарата дает возможность применять его при гипертонии сосудов головного мозга, ведь лекарство воздействует на просвет сосудов, максимально их расширяя. «Актовегин» не назначают при тяжелой форме гипертонической болезни, потому что маловероятно, что он сможет сбить высокие скачки давления, но при давлении, которое может незначительно подняться, окажется достаточно эффективным. Во избежание побочных симптомов не рекомендуется использовать описанный препарат при аритмии фибриллярного типа.
Вернуться к содержаниюБезопасность препарата
Препарат «Актовегин» относится к безопасным лекарствам, так как для его изготовления используются ткани животных, аналогичные Австралии, стране, в которой официально подтверждено отсутствие бешеной коровьей болезни. .Для производства Актовегина используется кровь телят — вещество, которое считается самым безопасным при изготовлении лекарств. Безопасность сырья зависит от возраста животного — чем моложе крупный рогатый скот, тем полезнее будет лекарственное вещество. Лекарственный препарат изготавливается из кровяной жидкости молодых телят, здоровых и питающихся отборным кормом.
Вернуться к содержаниюПоказания к применению
Препарат «Актовегин» рекомендуется применять для терапии патологических процессов, протекающих в организме человека:
- полинейропатия;
- нарушения обмена веществ в головном мозге;
- сосудистые периферические заболевания; пролежни;
- ожоги кожи;
- царапины;
- мокнущие язвы;
- лучевые поражения дермы;
- поражения кожи в результате лучевой терапии.
Инструкция по применению «Актовегина» под давлением
Применять препарат только после консультации с врачом.К каждой упаковке, содержащей лекарство, прилагается инструкция по применению, которую необходимо прочитать перед тем, как приступить к лечению. Кроме того, следует провести консультацию у врача, который на основании результатов диагностического обследования подберет форму лекарства и назначит необходимую дозировку в соответствии с поставленным диагнозом.Таблетки «Актовегин» пьют трижды в день первым делом перед едой. Таблетки перед приемом не разжевывают и не измельчают, глотают целиком, запивают водой очищенной. Продолжительность терапевтического курса обычно составляет от 4 до 6 недель.
Лекарство в виде мази и геля наносят тонким слоем на проблемные участки эпидермиса, повторяя процедуру 2-3 р. /24 часа. При необходимости в / в применении препарата дозировка определяется врачом индивидуально для каждого пациента.Обычно начальная дозировка раствора составляет 10-20 мл. За один раз допускается не более 5 мл, потому что «Актовегин» при передозировке сильно снижает артериальное давление.
Вернуться к оглавлениюПротивопоказания и побочные эффекты
| Когда не назначается? | негативные явления |
| Гиперчувствительность к компонентам Лекарство | сыпь на коже |
| Отек легких | Повышенный уровень кровотока до |
| кожный диабет | |
| декомпенсированная сердечная недостаточность | Отек |
| Грудное вскармливание | Анафилаксия |
| Олигурия | Лихорадка |
| Отсутствие в организме понижения давления мочи на обратное поступление мочи14 | 904 к содержаниюСрок продажи, хранения и истечения срока годностиПри покупке лекарственного средства рецепт врача является обязательным.Приобрести лекарство «Актовегин» можно в любой аптеке, но только по рецепту врача. Лекарство хранить в темном, недоступном для детей месте. |

 п.)
п.)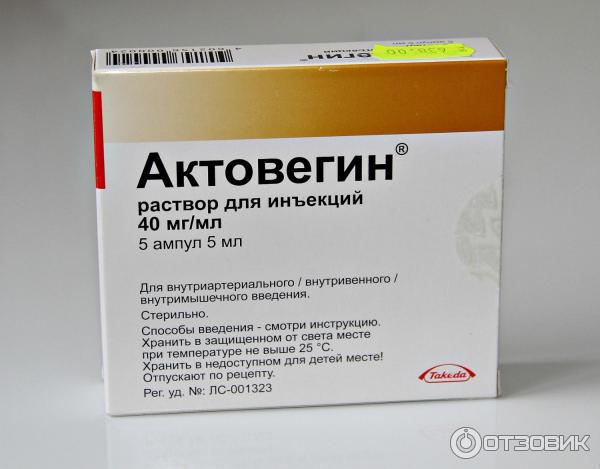

 При внутримышечном введении препарат входит достаточно болезненно.
При внутримышечном введении препарат входит достаточно болезненно.
 Увеличивает поглощение и вывод кислорода и глюкозы из крови, улучшает энергетический метаболизм клеток, питание ткани, понижает формирование лактата при ишемии.
Увеличивает поглощение и вывод кислорода и глюкозы из крови, улучшает энергетический метаболизм клеток, питание ткани, понижает формирование лактата при ишемии.